Diversidad en Ensayos Clínicos: Retos y Oportunidades para los Países Iberoamericanos
Diversity in Clinical Trials: Challenges and Opportunities for Ibero-American Countries
Nelson Santiago Vispo
1*Clinical Biotec SL. and Bionatura Journal. Madrid. 28029. Spain. Member of the Scientific Board, *Bionatura Journal* (role declared for transparency only).
2 Grupo de Investigación en Sanidad Animal y Humana (GISAH), Departamento de Ciencias de la Vida y la Agricultura, Universidad de las Fuerzas Armadas ESPE, Sangolquí 171103, Ecuador. Member of the Scientific Board, *Bionatura Journal* (role declared for transparency only).
*Correspondence: santiago@clinicalbiotec.com
*Correspondence: santiago@clinicalbiotec.com
RESUMEN
La población iberoamericana enfrenta desafíos significativos en su inclusión en los avances médicos internacionales, particularmente en los ensayos clínicos. Incrementar la diversidad en estos estudios es crucial para desarrollar tratamientos más seguros y eficaces, adaptados a las características genéticas, culturales y socioeconómicas únicas de la región. La falta de representatividad no solo perpetúa desigualdades en la atención médica, sino que también compromete la validez científica de los resultados. Se destaca la importancia de una medicina personalizada que considere factores genéticos y ambientales específicos, respaldada por investigaciones como las de la Red Iberoamericana de farmacogenética y Farmacogenómica (RIBEF), que abogan por la inclusión de la diversidad étnica en la farmacogenómica. Reformas en los criterios de selección y un enfoque colaborativo con instituciones locales son esenciales para garantizar la equidad en salud y mejorar el bienestar general en Iberoamérica.
Palabras clave. Ensayos clínicos, población iberoamericana, farmacogenómica, diversidad genética, medicina personalizada, inclusión, equidad en salud, RIBEF, factores socioculturales, investigación médica.
ABSTRACT
The Ibero-American population faces significant challenges in participating in international medical advancements, particularly in clinical trials. The Ibero-American population faces significant challenges in participating in international medical advancements, particularly in clinical trials. The enhancement of diversity in these studies is imperative for the development of safer and more efficacious treatments that are tailored to the distinctive genetic, cultural, and socioeconomic characteristics of the region. A lack of representation perpetuates healthcare inequalities and undermines scientific validity of findings. Research from organizations like Red Iberoamericana de farmacogenética y Farmacogenómica (RIBEF), which advocates for ethnic diversity in pharmacogenomics, shows how important personalized medicine is. Reforms to the participant selection criteria and collaborative approaches with local institutions are essential to ensure health equity and enhance overall well-being in Ibero-America.
Keywords. Clinical trials, Ibero-American population, pharmacogenomics, genetic diversity, personalized medicine, inclusion, health equity, RIBEF, sociocultural factors, medical research.
Impacto de la Diversidad Genética y Cultural
La población iberoamericana enfrenta importantes retos para participar en los avances médicos globales, especialmente en los ensayos clínicos. Fomentar la diversidad en estos estudios es esencial para crear tratamientos más seguros y efectivos, adaptados a las particularidades genéticas, culturales y sociales de la región. La limitada representación no solo amplifica las desigualdades en salud, sino que también compromete la validez científica de los hallazgos.
Las disparidades sociales, tales como el acceso a la atención médica, la educación, el apoyo social y la influencia del estilo de vida, afectan significativamente en los resultados del tratamiento. Las personas con un acceso limitado a la atención médica o con bajos niveles de alfabetización en salud pueden enfrentar retos para recibir y comprender la atención médica adecuada. Los factores culturales, tales como las creencias sobre la salud, las prácticas de comunicación y las preferencias de tratamiento, también influyen en las decisiones de tratamiento y la adherencia. Los profesionales de la salud deben ser culturalmente sensibles y tener en cuenta las perspectivas de los pacientes para ofrecer una atención eficaz. 1
Las diferencias genéticas desempeñan un papel relevante en la respuesta de un individuo a los tratamientos. La investigación de la farmacogenómica examina la influencia de los genes en el proceso de metabolización de los medicamentos, lo que conlleva a variaciones en la eficacia y los efectos secundarios. Asimismo, la predisposición genética a las patologías y la respuesta al tratamiento varían entre individuos. Determinar estos factores genéticos permite enfoques de tratamiento personalizados y puede mejorar los resultados de los pacientes. Descubrir la conexión entre los factores sociales, culturales y genéticos es fundamental para ofrecer una atención médica equitativa y mejorar los resultados de salud para todos. 2
Las últimas tres décadas han sido testigos de un intenso interés en la predictibilidad de la respuesta a la medicación que se puede atribuir a la composición genética de los pacientes, para asegurar la eficacia y seguridad de los fármacos existentes y nuevos 3. El estudio de la mezcla de ancestros en las poblaciones humanas está revolucionando la medicina. Nos permite comprender mejor por qué las personas reaccionan de manera diferente a los mismos medicamentos. La información sobre la ascendencia genética puede ser útil para identificar individuos con mayor riesgo a ciertas enfermedades y para desarrollar tratamientos más efectivos y precisos. Esta variabilidad en la respuesta farmacológica se debe a diferencias genéticas que influyen en procesos como la absorción, el metabolismo, la distribución y la eliminación de los fármacos.
Representación Étnica en Iberoamérica: Estado Actual
Para abordar esta problemática, resulta imperativo modificar los criterios de selección de los participantes en los estudios. Debemos asegurar la inclusión de personas con diferentes orígenes y características para obtener resultados más precisos y equitativos. De esta manera, los procedimientos médicos serán seguros y eficaces para todos, independientemente de su origen o situación social. 4
Este problema es particularmente relevante en los países iberoamericanos, donde las diferencias socioeconómicas, culturales y genéticas pueden tener un efecto significativo en la eficacia y seguridad de las intervenciones médicas. Las tendencias históricas evidencian una preferencia por las poblaciones de estudio heterogéneas, ignorando con frecuencia los desafíos sanitarios que afrontan diversos grupos étnicos y sociales. Esto podría generar datos incompletos que no representen la complejidad de la salud humana. 4
Por lo tanto, es esencial reconsiderar los métodos y procesos de reclutamiento actuales para establecer marcos más inclusivos que fomenten una representación integral en la investigación clínica. La supervisión de estas deficiencias no solo mejora la precisión de los resultados de los estudios, sino también fomenta la equidad en la salud y facilita el desarrollo de tratamientos médicos seguros y eficientes que se adapten a la diversidad demográfica de estas regiones.
Avances y Barreras en los Ensayos Clínicos Multirregionales
El Consejo Internacional de Armonización de Requisitos Técnicos para Productos farmacéuticos de uso Humano (ICH) desempeña un papel fundamental en la búsqueda de productos farmacéuticos seguros y eficaces para todas las poblaciones. La presente iniciativa global congrega a las autoridades reguladoras y la industria farmacéutica con el propósito de armonizar los aspectos científicos y técnicos del desarrollo y registro de medicamentos. 5
La colaboración entre organismos reguladores de la Unión Europea, Japón, Estados Unidos y otras naciones, así como expertos de la industria farmacéutica, tiene como objetivo alcanzar una mayor uniformidad en la interpretación y aplicación de directrices y requisitos técnicos.
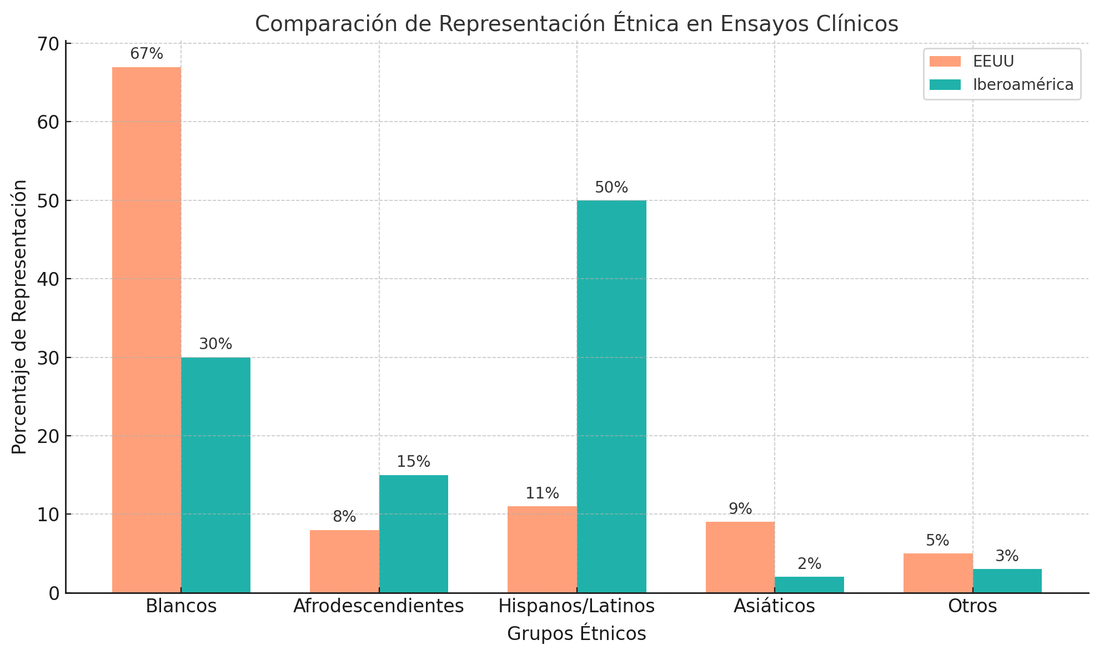
Figura 1. Comparación de la representación étnica en ensayos clínicos entre Estados Unidos e Iberoamérica. Los participantes blancos dominan en Estados Unidos, mientras que en Iberoamérica prevalecen los hispanos/latinos y mestizos Trials per year- World (1999-2021) . Sin embargo, los grupos afrodescendientes y otros siguen estando subrepresentados en ambas regiones.6, 7
Armonización de estándares
La ICH se enfoca en la elaboración de directrices que brinden recomendaciones sobre diversos aspectos del desarrollo de medicamentos, tales como:
- Eficacia y Seguridad: Se establecen directrices acerca de la garantía de calidad, el control de la seguridad, el diseño de ensayos clínicos y la seguridad farmacológica.
- Eficacia: metodología de ensayos clínicos; análisis de datos e informes; metodología de ensayos clínicos; análisis de datos e informes.
- Temas multidisciplinares: En materia electrónica; estudios pediátricos y bioética.
A pesar de no ser jurídicamente vinculantes, las directrices de la ICH son muy influyentes y ampliamente adoptadas por las agencias reguladoras de todo el mundo. Dado que la ICH armoniza los requisitos técnicos para el registro de productos farmacéuticos, la ICH facilita el desarrollo y la disponibilidad de medicamentos seguros y eficaces para todos, independientemente de su origen étnico o características genéticas.
Directrices para la diversidad
La ICH ha elaborado directrices específicas para fomentar la inclusión de diversas poblaciones en la investigación clínica de la ICH:
ICH E5: Factores étnicos en la aceptabilidad de datos clínicos extranjeros: Estas estrategias analizan la influencia de los factores étnicos en la aceptabilidad de los datos clínicos extranjeros. Se recalca la importancia de tener en cuenta las diferencias étnicas en la respuesta al fármaco y la prevalencia de la enfermedad al momento de diseñar y llevar a cabo ensayos clínicos.
ICH E11: Planes de diversidad para mejorar la inscripción de participantes de poblaciones raciales y étnicas infrarrepresentadas en ensayos clínicos: Ofrece recomendaciones a los patrocinadores y enfatiza la importancia de incluir poblaciones diversas en los ensayos clínicos e identificar las poblaciones infrarrepresentadas dentro de su población diana específica y región geográfica.
ICH E17: Ensayos clínicos multirregionales: Esta directriz propone el diseño y la ejecución de ensayos clínicos multirregionales. Cabe destacar la importancia de incluir poblaciones diversas en estos ensayos para asegurar que los resultados sean generalizables a todas las poblaciones.
ICH E8 (R1): Consideraciones generales para los ensayos clínicos: Esta directriz establece criterios generales para el diseño y la realización de ensayos clínicos. Se establecen recomendaciones para incluir poblaciones diversas para garantizar la seguridad y eficacia de los tratamientos en todas las poblaciones.
Visión general de los ensayos clínicos y su importancia en la investigación médica
Los estudios clínicos constituyen la base fundamental de la medicina basada en la evidencia, ya que proporcionan información relevante para las prácticas clínicas y las políticas sanitarias. Estos estudios, debidamente diseñados, evalúan con rigor nuevos tratamientos, intervenciones o procedimientos diagnósticos mediante metodologías sistemáticas que garantizan la validez y fiabilidad de sus resultados. Al establecer grupos de control y utilizar técnicas de aleatorización, los ensayos clínicos minimizan los sesgos y proporcionan un nivel de rigor científico esencial para el avance del conocimiento médico. 6,7
Los ensayos son fundamentales para comprender la eficacia de las intervenciones sanitarias en poblaciones diversas y la variabilidad de las respuestas al tratamiento entre los diferentes grupos demográficos, especialmente en contextos iberoamericanos. En consecuencia, la inclusión de la diversidad en los estudios clínicos incrementa la generalizabilidad de los hallazgos. Esto fomenta la inclusión, que es fundamental para la realización ética de la investigación médica y la prestación óptima de asistencia sanitaria .8
Estado actual de los ensayos clínicos en los países iberoamericanos.
Los países iberoamericanos han mostrado un compromiso por mejorar la metodología de los ensayos clínicos, con el objetivo de aumentar la integridad de la investigación y la seguridad de los participantes. A pesar de los notables progresos, los investigadores se enfrentan a numerosas dificultades que pueden afectar la efectividad de los estudios. Los diferentes niveles de apoyo infraestructural en estos países contribuyen a incoherencias en la calidad de los datos y el reclutamiento de participantes en estos países, lo que plantea dudas acerca de la generalizabilidad de los resultados. 9
Además, las diferencias culturales y las barreras lingüísticas dificultan la comunicación eficaz en el entorno clínico, lo que afecta al cumplimiento de los pacientes y a los resultados de los estudios.
A medida que la comunidad científica global reconoce la relevancia de incorporar individuos diversos en los ensayos clínicos, los Estados Unidos se encuentran en una situación de dificultad. Poseen características demográficas que pueden proporcionar información valiosa acerca de la patología de la enfermedad y su respuesta al tratamiento. No obstante, deben enfrentar desafíos estructurales que dificultan su participación en el panorama general de la investigación. 10
Análisis de la representación demográfica en los ensayos clínicos existentes.
Aunque los estudios sobre poblaciones de todo el mundo son cada vez más frecuentes, algunas regiones aún están subrepresentadas, en particular el continente africano y Oriente Medio, al contrario de las poblaciones europeas y del este asiático 12. Una evaluación minuciosa de los estudios clínicos existentes evidencia significativas discrepancias en la representación demográfica, especialmente en los grupos infrarrepresentados en la nación de Iberoamérica. Las disparidades pueden generar resultados sesgados que no reflejan con precisión a las poblaciones más amplias, lo que compromete la eficacia y seguridad de los tratamientos en diversos segmentos demográficos. Los factores como el nivel socioeconómico, la etnia y la ubicación geográfica pueden generar sesgos en el reclutamiento que favorecen a poblaciones específicas, especialmente a las más accesibles o convenientes para los investigadores. 11
En consecuencia, los datos obtenidos pueden no ser generalizables, lo cual dificulta la adopción de los descubrimientos a las comunidades marginadas que pueden experimentar resultados sanitarios dispares. La falta de representación de estos grupos incrementa las desigualdades sanitarias existentes y obstaculiza el progreso de los conocimientos médicos. La supervisión de estas deficiencias es fundamental para la investigación clínica y para asegurar que los beneficios de los avances médicos se extiendan equitativamente a todos los estratos demográficos. 12
El impacto de la diversidad de la población en los resultados de los ensayos clínicos.
La diversidad de la población tiene un impacto significativo en los resultados de los ensayos clínicos, aumentando la validez y la aplicabilidad de los hallazgos. La inclusión de participantes con diversas características genéticas, ambientales y socioeconómicas amplía la generalizabilidad de los estudios y permite identificar factores que influyen en las respuestas al tratamiento, incluyendo posibles efectos secundarios no previstos. Esta pluralidad expone disparidades sanitarias que, de otro modo, podrían pasar desapercibidas, ofreciendo una perspectiva integral sobre la seguridad y eficacia de las intervenciones.
Desde un punto de vista ético, garantizar la representación diversa en los ensayos clínicos es crucial para que los beneficios de la investigación sean accesibles a todos los segmentos de la población. La ausencia de esta diversidad perpetúa desigualdades existentes, particularmente en los países iberoamericanos, donde las comunidades enfrentan retos únicos en materia de salud. Por lo tanto, promover la inclusión en estos estudios no solo responde a un imperativo ético, sino que también fortalece el rigor científico y mejora la calidad de la atención sanitaria 13
Cómo influyen los factores genéticos y ambientales en la eficacia y seguridad de los medicamentos
La exploración de la interacción entre las características genéticas y las variables ambientales resulta crucial para evaluar la eficacia y seguridad de los medicamentos en diversas poblaciones. Los polimorfismos genéticos pueden alterar significativamente la farmacocinética y la farmacodinámica, lo que a su vez puede provocar variaciones en las respuestas terapéuticas y los efectos adversos entre individuos. Por ejemplo, las variaciones en las enzimas del citocromo P450, responsables del metabolismo de los fármacos, pueden provocar respuestas subóptimas o reacciones tóxicas, dependiendo de la composición genética de cada individuo. Asimismo, factores ambientales como la dieta, la situación socioeconómica y las condiciones de salud coexistentes pueden dificultar aún más estas interacciones, por lo tanto, es fundamental tener en cuenta el contexto holístico del paciente. 14
Existen algunos estudios que relacionan loss de admixture y la farmacogenómica en poblaciones con un origen Iberoamericano. Uno de estos primeros estudios establece la asociación entre la ascendencia europea y la diabetes tipo 1 lo que indica la contribución de la etnicidad a las diferencias de incidencia 17. Otra investigación más reciente es un estudio farmacogenético realizado en la República Dominicana, analizando la variabilidad de los genes CYP2D6, CYP2C9 y CYP2C19 en 197 voluntarios sanos, mostrando una alta mezcla genética en la población dominicana, con un componente africano mayor al esperado y superior al de otras poblaciones latinoamericanas. Se encontraron frecuencias alélicas específicas que influyen en la actividad enzimática de estos genes, con implicaciones para el metabolismo de fármacos.15
El Consorcio RIBEF-CEIBA (Consorcio de Estudios en Interacción Biomédica y Ancestralidad) desempeña un papel clave en la investigación de cómo las variaciones genéticas y ancestrales influyen en la farmacogenómica en Iberoamérica. Estas organizaciones se enfocan en optimizar la implementación de la medicina personalizada, con un énfasis particular en incluir la etnicidad en el desarrollo de guías farmacogenéticas para la práctica clínica, la investigación y la regulación. Su objetivo es reducir la brecha biotecnológica global y garantizar que las poblaciones históricamente subrepresentadas tengan acceso equitativo a tratamientos personalizados y seguros.
La Red Iberoamericana de Farmacogenética y Farmacogenómica (RIBEF), en colaboración con CEIBA, ha liderado iniciativas innovadoras como el estudio MESTIFAR, que analizó a más de 6,000 individuos de diversas etnias en Iberoamérica. Este estudio pionero, el primero en examinar una cohorte tan heterogénea, ha demostrado la relevancia del factor étnico en la respuesta a los fármacos y cuestionado la idoneidad de las dosis estandarizadas a nivel global. Estas investigaciones recalcan la importancia de adaptar los tratamientos farmacológicos a las características genéticas y ancestrales de cada población.
Ambos estudios destacan la necesidad de considerar la etnicidad y la ancestralidad genética en la farmacogenómica, ya que las recomendaciones actuales, basadas mayoritariamente en poblaciones europeas, podrían no ser aplicables a grupos como los latinoamericanos. Se subraya, además, la urgencia de investigar más a fondo las poblaciones con ancestría africana, como las de Cuba y República Dominicana, para identificar variantes genéticas clave y estratificar mejor a los individuos en riesgo.
Los expertos han enfatizado la importancia de incluir el factor étnico en los estudios de seguridad de medicamentos, con el objetivo de que la medicina personalizada beneficie también a las poblaciones autóctonas de América Latina. Estas iniciativas reflejan el compromiso de la RIBEF y CEIBA de fomentar la equidad en salud mediante una investigación clínica inclusiva y representativa.
El programa MESTIFAR ha demostrado que es importante considerar la etnicidad para asegurar los medicamentos seguros. La "Declaración" con las conclusiones del estudio se ha presentado al Consejo de Organizaciones Internacionales de Ciencias Médicas (CIOMS) y a la Organización Mundial de la Salud (OMS) con el fin de fomentar la inclusión de la etnicidad en el desarrollo de fármacos y tratamientos más seguros y eficaces. La RIBEF se enfoca en que la medicina personalizada beneficie a todos los individuos, fomentando la inclusión del factor étnico en las investigaciones y guías de administración farmacológica.17
En el contexto de los ensayos clínicos, especialmente en los países iberoamericanos, la diversidad de la población aumenta la generalizabilidad de los resultados y optimiza los procesos de desarrollo de fármacos en el contexto de los ensayos clínicos. Esto se debe a que garantiza la representación adecuada de las influencias multifactoriales en la respuesta al fármaco.
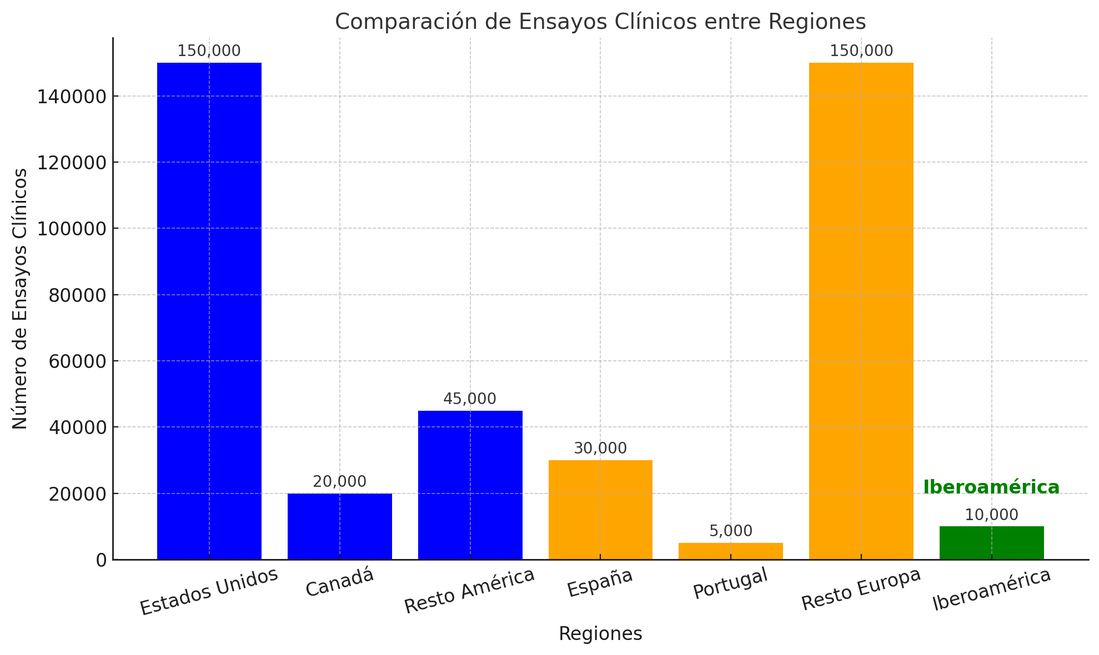
Figura 2 Comparación del volumen de ensayos clínicos entre Europa, América e Iberoamérica, destacando las diferencias en capacidad y enfoque de investigación. El gráfico subraya el predominio de Estados Unidos y el resto de Europa, con una contribución más modesta de Iberoamérica.18
El volumen de ensayos clínicos muestra marcadas diferencias entre regiones. En América, Estados Unidos lidera ampliamente con más de 150,000 ensayos registrados, reflejando su robusta infraestructura e inversión en investigación médica, seguido de Canadá. En contraste, el resto de los países americanos, incluyendo a Iberoamérica (Brasil, México, Argentina, entre otros), alcanzan entre 10,000 y 50,000 ensayos combinados, evidenciando limitaciones estructurales y de financiamiento. En Europa, Alemania, Reino Unido y Francia concentran la mayor parte de los estudios, con cerca de 100,000 ensayos combinados, mientras que España y Portugal destacan por su representación proporcionalmente alta en áreas como enfermedades metabólicas y cardiovasculares.
El enfoque en la diversidad y la población también varía. En Estados Unidos, la diversidad étnica es un factor clave, aunque persisten retos para incluir a comunidades marginadas, especialmente latinas. En Iberoamérica, las barreras culturales e infraestructurales restringen la representatividad de sus ensayos clínicos. En Europa, la inclusión de poblaciones diversas lidera el panorama, con avances en España y Portugal en áreas genéticas y metabólicas, aunque con desafíos en representar a las poblaciones migrantes.
En términos de áreas prioritarias, América y Europa comparten un enfoque en enfermedades no transmisibles como el cáncer y la diabetes, aunque Europa muestra un creciente interés en enfermedades raras y terapias genéticas. Por su parte, Iberoamérica enfrenta un enfoque en enfermedades infecciosas y metabólicas, reflejando los desafíos específicos de su salud pública.
Estos resultados resaltan la importancia de mejorar la infraestructura de investigación y fomentar colaboraciones internacionales en Iberoamérica, promoviendo la inclusión de poblaciones marginadas para garantizar estudios éticos y representativos.18
CONCLUSIONES
Considerando la relevancia de la heterogeneidad de la población en los estudios clínicos, es evidente que un enfoque homogéneo en la investigación médica es inadecuado. Los factores genéticos, ambientales y socioculturales inherentes a las diversas poblaciones, especialmente en los países iberoamericanos, requieren metodologías que tengan en cuenta estas variables específicas. Esta pluralidad mejora la validez de los resultados de los estudios y promueve una mayor equidad en el acceso a la atención médica y la eficacia de los tratamientos.
Las repercusiones de estos descubrimientos no solo se refieren a la seguridad clínica, sino también a las premisas éticas. Las prácticas de investigación integradoras pueden reducir las disparidades sanitarias que enfrentan las comunidades infrarrepresentadas a través de prácticas de investigación integradoras.
En consecuencia, fomentar la pluralidad en los ensayos clínicos constituye un requisito normativo y un imperativo ético que mejora el rigor científico y la justicia social en la investigación médica. Se destaca la necesidad de implementar reformas políticas que garanticen una representación plural en los ensayos clínicos en la nación de Iberoamérica.
Resumen de conclusiones claves y recomendaciones para futuros ensayos clínicos en contextos iberoamericanos
La inclusión de cohortes de individuos diversos en los ensayos clínicos ha evidenciado una significativa disparidad en la eficacia y seguridad de los fármacos, especialmente en la región de Iberoamérica. La heterogeneidad de los participantes en estudios previos genera resultados sesgados que no reflejan con exactitud las variaciones farmacológicas en estas poblaciones.
Para asegurar la validez de los resultados, es crucial que los ensayos clínicos en Iberoamérica adapten sus metodologías considerando las características de salud, ambientales y culturales de sus poblaciones
Se aconseja establecer conexiones de colaboración entre empresas farmacéuticas globales y instituciones de investigación regionales. Así se garantiza que los estudios sean culturalmente relevantes y éticos. Asimismo, la inversión en iniciativas de divulgación comunitaria puede mejorar la participación en los ensayos. En conclusión, el compromiso con la diversidad en la investigación clínica propiciará avances médicos más eficaces y mejorará la atención sanitaria en la región.
REFERENCIAS
1. Ramos TI, Castro KA, Escalante LS, Vispo NS. Advances in Clinical Research in Ecuador. Ther Innov Regul Sci. 2017 May;51(3):307–13.
2. Communications. Integra IT. 2024 [cited 2024 Nov 9]. Por qué importa la diversidad en los ensayos clínicos. Available from: https://www.integrait.co/es/por-que-importa-la-diversidad-en-los-ensayos-clinicos/
3. Kalman L, Agúndez J, Appell ML, Black J, Bell G, Boukouvala S, et al. Pharmacogenetic allele nomenclature: International workgroup recommendations for test result reporting. Clin Pharma and Therapeutics. 2016 Feb;99(2):172–85.
4. Fatumo S, Chikowore T, Choudhury A, Ayub M, Kuchenbäcker K. A Roadmap to Increase Diversity in Genomic Studies.
5. Abraham J. International Conference On Harmonisation Of Technical Requirements For Registration Of Pharmaceuticals For Human Use. In: Tietje C, Brouder A, editors. Handbook of Transnational Economic Governance Regimes [Internet]. Brill | Nijhoff; 2010 [cited 2024 Nov 8]. p. 1041–53. Available from: https://brill.com/view/book/edcoll/9789004181564/Bej.9789004163300.i-1081_085.xml
6. Desafíos en la representación étnica en ensayos clínicos: Hacia una mayor equidad en la investigación médica | Medby [Internet]. 2024 [cited 2024 Nov 24]. Available from: https://medby.org/desafios-en-la-representacion-etnica-en-ensayos-clinicos-hacia-una-mayor-equidad-en-la-investigacion-medica/
7. Taparra K, Benavente R, Shih JJ, Gimmen MY, Tominez P, Kekumano K, et al. Race and Ethnicity Representation in Phase 2/3 Oncology Clinical Trial Publications: A Systematic Review. JAMA Health Forum. 2024 Jun 7;5(6):e241388.
8. Alowais SA, Alghamdi SS, Alsuhebany N, Alqahtani T, Alshaya AI, Almohareb SN, et al. Revolutionizing healthcare: the role of artificial intelligence in clinical practice. BMC Med Educ. 2023 Sep 22;23(1):689.
9. Michos ED, Reddy TK, Gulati M, Brewer LC, Bond RM, Velarde GP, et al. Improving the enrollment of women and racially/ethnically diverse populations in cardiovascular clinical trials: An ASPC practice statement. American Journal of Preventive Cardiology. 2021 Dec 1;8:100250.
10. Peñas-LLedó E, Terán E, Sosa-Macías M, Galaviz-Hernández C, Gil JP, Nair S, et al. Challenges and Opportunities for Clinical Pharmacogenetic Research Studies in Resource-limited Settings: Conclusions From the Council for International Organizations of Medical Sciences–Ibero-American Network of Pharmacogenetics and Pharmacogenomics Meeting. Clinical Therapeutics. 2020 Aug 1;42(8):1595-1610.e5.
11. Rodrigues-Soares F, Peñas-Lledó EM, Tarazona-Santos E, Sosa-Macías M, Terán E, López-López M, et al. Genomic Ancestry, 2D6, 2C9, and 2C19 Among Latin Americans. Clinical Pharmacology & Therapeutics. 2020;107(1):257–68.
12. LLerena A, Naranjo MEG, Rodrigues-Soares F, Penas-LLedó EM, Fariñas H, Tarazona-Santos E. Interethnic variability of CYP2D6 alleles and of predicted and measured metabolic phenotypes across world populations. Expert Opinion on Drug Metabolism & Toxicology. 2014 Nov;10(11):1569–83.
13. Salas-Hernández A, Galleguillos M, Carrasco M, López-Cortés A, Redal MA, Fonseca-Mendoza D, et al. An updated examination of the perception of barriers for pharmacogenomics implementation and the usefulness of drug/gene pairs in Latin America and the Caribbean. Front Pharmacol. 2023 May 11;14:1175737.
14. Gallego-Perez D, Wardle J, Declercq E, Wirtz V, Saper R, Barnes L. Therapeutic pluralism policies in latin america: advances, gaps, and opportunities towards inclusive, people-centered health care systems. Popul Med [Internet]. 2023 Apr 26 [cited 2024 Nov 9];5(Supplement). Available from: http://www.populationmedicine.eu/Therapeutic-pluralism-policies-in-latin-america-advances-gaps-and-opportunities-towards,164473,0,2.html
15. Bonilla CE, Montenegro P, O’Connor JM, Hernando-Requejo O, Aranda E, Pinto Llerena J, et al. Ibero-American Consensus Review and Incorporation of New Biomarkers for Clinical Practice in Colorectal Cancer. Cancers. 2023 Sep 1;15(17):4373.
16. Principi N, Petropulacos K, Esposito S. Impact of Pharmacogenomics in Clinical Practice. Pharmaceuticals. 2023 Nov 13;16(11):1596.
17. Diaz-Horta O, Cintado A, Fernandez-De-Cossio ME, Nazabal M, Ferrer A, Roca J, et al. Relationship of type 1 diabetes to ancestral proportions and HLA DR/DQ alleles in a sample of the admixed Cuban population. Annals of Human Biology. 2010 Nov;37(6):778–88.
18. Guevara M, Rodrigues-Soares F, De La Cruz CG, De Andrés F, Rodríguez E, Peñas-Lledó E, et al. Afro-Latin American Pharmacogenetics of CYP2D6, CYP2C9, and CYP2C19 in Dominicans: A Study from the RIBEF-CEIBA Consortium. Pharmaceutics. 2024 Oct 30;16(11):1399.
19. Red Ribef [Internet]. [cited 2024 Nov 10]. Inicio. Available from: https://redribef.org
20. Number of clinical trials by year, location, disease, phase, age and sex of trial participants [Internet]. [cited 2024 Nov 24]. Available from: https://www.who.int/observatories/global-observatory-on-health-research-and-development/monitoring/number-of-trial-registrations-by-year-location-disease-and-phase-of-development-feb-2022
Received: October 15, 2024 / Accepted: November 24, 2024 / Published: December 15, 2024
Citation: Santiago Vispo N, and Ramos T. Diversidad en Ensayos Clínicos: Retos y Oportunidades para los Países Iberoamericanos. Bionatura journal. 2024;1(4):1. doi: 10.70099/BJ/2024.01.04.1
Additional information Correspondence should be addressed to santiago@cliniclbiotec.com
Peer review information. Bionatura thanks anonymous reviewer(s) for their contribution to the peer review of this work using https://reviewerlocator.webofscience.com/
ISSN.3020-7886
All articles published by Bionatura Journal are made freely and permanently accessible online immediately upon publication, without subscription charges or registration barriers.
Publisher's Note: Bionatura Journal stays neutral concerning jurisdictional claims in published maps and institutional affiliations.
Copyright: © 2024 by the authors. They were submitted for possible open-access publication under the terms and conditions of the Creative Commons Attribution (CC BY) license (https://creativecommons.org/licenses/by/4.0/).




