Optimización del Crecimiento Mixotrófico de Chlorella sp. mediante la Valorización de Derivados Lácteos: Análisis Cinético, Bromatológico y de Costos
Optimizing Mixotrophic Growth of Chlorella sp. through Dairy By-product Valorization: Kinetic, Bromatological, and Cost-Benefit Analysis

Geovanna Elizabeth Guevara Figueroa 

Pedro José Rachid Romero Saker

Pedro José Rachid Romero Saker
¹ Universidad de las Fuerzas Armadas ESPE, Ecuador
² Escuela Superior Politécnica Agropecuaria de Manabí Manuel Félix López (ESPAM MFL), Ecuador
² Escuela Superior Politécnica Agropecuaria de Manabí Manuel Félix López (ESPAM MFL), Ecuador
Correspondencia: edmorales@espam.edu.ec; Tel.: +593 96 733 1848
RESUMEN
La producción sostenible de microalgas requiere medios de cultivo de bajo costo y alta eficiencia. Este estudio evaluó el crecimiento, la composición de pigmentos y el perfil bromatológico de Chlorella sp. aislada de efluentes lácteos, comparando sistemas fotoautotróficos (fertilizante Nitrofoska) y mixotróficos (yogurt natural semidescremado). En condiciones autotróficas, la densidad máxima fue de 26×106 cel⋅mL−1 (3 mL⋅L−1 de fertilizante, 166.66 μmol⋅m−2⋅s−1). El cultivo mixotrófico con yogurt al 5% (v/v) alcanzó una densidad superior a 47.3×106 cel⋅mL−1, con una productividad de biomasa seca de 3.16 g⋅L−1, superando significativamente a los 0.81 g⋅L−1 del sistema autotrófico en el escalamiento. El análisis proximal reveló un contenido proteico del 38,3% en mixotrofía, lo que mantiene la calidad nutricional. Aunque el costo por gramo de biomasa fue ligeramente superior en mixotrofía (0.04 vs 0.023 USD⋅g−1), la alta productividad sugiere una viabilidad técnica superior para biorrefinerías. Estos resultados demuestran que el yogurt es un sustrato orgánico eficaz para la intensificación de cultivos de Chlorella, al integrar la valorización de residuos con la producción de biomasa de alto valor proteico.
Palabras claves. Chlorella sp., Mixotrofía, Valorización de residuos lácteos, Biomasa microalgal, Cinética de crecimiento, Biorrefinería.
ABSTRACT
Sustainable microalgae production requires cost-effective, high-efficiency culture media. This study evaluated the growth, pigment composition, and bromatological profile of Chlorella sp. isolated from dairy effluents, comparing photoautotrophic (Nitrofoska fertilizer) and mixotrophic (low-fat yogurt) systems. Under autotrophic conditions, maximum density reached 26×106cells⋅mL−1 ( 3mL⋅L−1 fertilizer, 166.66μmol⋅m−2⋅s−1). Mixotrophic cultivation with 5% (v/v) yogurt achieved a higher density of 47.3×106cells⋅mL−1, yielding a dry biomass productivity of 3.16g⋅L−1, significantly outperforming the 0.81g⋅L−1 was obtained in the autotrophic system during scale-up. Proximal analysis revealed a protein content of 38.3% in mixotrophy, preserving nutritional quality. Although the cost per gram of biomass was slightly higher in mixotrophy ( 0.04 vs 0.023USD⋅g−1), the enhanced productivity suggests superior technical viability for biorefineries. These results demonstrate that yogurt serves as an effective organic substrate for intensifying Chlorella cultures, integrating waste valorization with high-protein biomass production.
Sustainable microalgae production requires cost-effective, high-efficiency culture media. This study evaluated the growth, pigment composition, and bromatological profile of Chlorella sp. isolated from dairy effluents, comparing photoautotrophic (Nitrofoska fertilizer) and mixotrophic (low-fat yogurt) systems. Under autotrophic conditions, maximum density reached
Keywords. Chlorella sp., Mixotrophy, Dairy waste valorization, Microalgal biomass, Growth kinetics, Biorefinery.
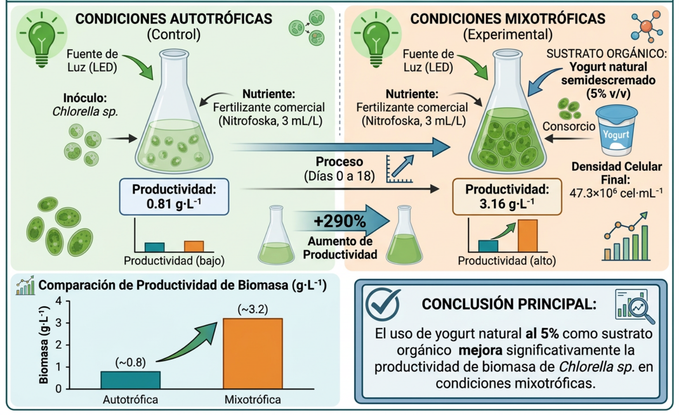
Resumen gráfico del estudio. Comparación esquemática entre el cultivo autotrófico (control) y el cultivo mixotrófico (experimental) de Chlorella sp. utilizando fertilizante comercial Nitrofoska (3 mL·L⁻¹) y yogurt natural semidescremado al 5 % (v/v) como sustrato orgánico. En condiciones mixotróficas se observó una mayor densidad celular final y una productividad de biomasa seca superior a la del sistema autotrófico (3.16 vs. 0.81 g·L⁻¹), lo que indica el potencial del suplemento lácteo para intensificar la producción de biomasa microalgal bajo condiciones de laboratorio.
INTRODUCCIÓN
Las microalgas son organismos fotosintéticos con estructura celular simple que viven en ambientes acuáticos, donde obtienen los nutrientes necesarios para crecer; su crecimiento es rápido en comparación con otros organismos, por eso pueden generar grandes cantidades de biomasa por unidad de superficie 1. Desde hace siglos el ser humano las usa como alimento, medicamento y biofertilizante, también se emplean en alimentos funcionales porque aumentan el valor nutricional de productos tradicionales y aportan proteínas, ácidos grasos, minerales y vitaminas que favorecen la salud animal y humana 2.
Algunas especies producen compuestos bioactivos a los que se les atribuyen propiedades farmacológicas, aunque los mecanismos de acción no siempre se entienden bien 3. En la actualidad existe interés económico por las microalgas debido a la presencia de componentes celulares con valor comercial 4.
Cerca del 90 % del peso seco de una célula microalgal corresponde a proteínas, lípidos y carbohidratos, la proteína suele ser la fracción principal de la biomasa, seguida por lípidos y carbohidratos, pero esta composición cambia según la especie y las condiciones de cultivo 5. Las microalgas también se estudian por su capacidad de captar CO2 atmosférico y por la producción de biocombustibles a partir de sus aceites; parece que esta combinación ofrece una alternativa energética viable, aunque su aplicación depende todavía de factores técnicos y económicos 6.
Entre los géneros con mayor interés industrial se encuentran Chlorella, utilizada en nutrición humana, acuacultura y cosmética; Dunaliella salina, empleada en nutrición y en la obtención de beta-carotenos; Arthrospira, usada en nutrición humana y animal y en la producción de ficobiliproteínas; Aphanizomenon flos-aquae, destinada al consumo humano; Haematococcus pluvialis, asociada a la acuacultura y a la producción de astaxantina; y en cambio, Crypthecodinium cohnii y Schizochytrium sp., son utilizadas para obtener DHA, un ácido graso esencial omega-3 7.
Los medios de cultivo de algunas microalgas permiten tasas de crecimiento superiores a las observadas en otras especies vegetales, lo que favorece la producción de biomasa, pero a escala industrial existen limitaciones relacionadas con el costo de los componentes del medio y el aumento del precio de los fertilizantes inorgánicos. Los cultivos mixotróficos pueden generar más biomasa que los sistemas autotróficos y heterotróficos; ya que utilizan al mismo tiempo la energía lumínica y sustratos orgánicos 8.
En Ecuador, la producción de microalgas en condiciones mixotróficas con derivados lácteos aparece como una opción interesante por la posible reducción de costos asociada al uso de nutrientes inorgánicos. En este trabajo se evaluó el potencial nutricional del yogurt como sustrato para la producción de biomasa de la microalga Chlorella sp., en un sistema de cultivo con potencial para la formación de consorcios entre la microalga y los microorganismos presentes en el derivado lácteo 9. El estudio presenta bases experimentales para explorar aplicaciones biotecnológicas relacionadas con la producción de biomasa microalgal, aunque su alcance se limita a condiciones controladas de laboratorio. El principal objetivo del estudio fue el de proponer una mejora en el costo-beneficio para producción industrial, puesto que existen microalgas con gran capacidad de ser cultivadas con sustratos orgánicos y la utiliza-ción simultánea de luz demostrando su capacidad mixotrófica.
MATERIALES Y MÉTODOS
Los ensayos experimentales se realizaron en el Laboratorio del Centro de Investigación y Valoración de la Biodiversidad (CIVABI) de la Universidad Politécnica Salesiana, campus Girón, Quito, Ecuador (latitud −0.208348; longitud −78.487452). La microalga Chlorella sp. fue obtenida a partir de un efluente lácteo procedente de la empresa ECUALAC (Machachi, Ecuador) y aislada mediante inoculación en medio fertilizante foliar Nitrofoska (N total 10 %, P2O5 4.0 %, K₂O 7.0 %, MgO 2.0 %, S 0.8 %, Fe 70 ppm, Co 12 ppm y Mo 1 ppm) bajo iluminación continua. La identidad del cultivo se verificó mediante observación microscópica considerando características morfológicas, patrón de crecimiento y pigmentación celular.
El escalamiento del inóculo se realizó en sistema discontinuo incrementando progresivamente el volumen desde 20 mL hasta 2500 mL en medio Nitrofoska (3 mL/L), manteniendo aireación continua y temperatura de 21±2 °C. Todos los experimentos se desarrollaron bajo un diseño completamente al azar. En el primer ensayo se evaluaron concentraciones de Nitrofoska de 1, 2 y 3 mL/L en frascos de 500 mL con 250 mL de medio de cultivo e inóculo inicial de 1×10⁶ células/mL, bajo flujo fotónico de 115 μmol m-2 s-1, fotoperiodo 12:12 h y aireación continua. En el segundo ensayo se evaluó el crecimiento a diferentes intensidades luminosas (92.59 y 166.66 μmol m-2 s-1) utilizando Nitrofoska 3 mL/L, con tres repeticiones por tratamiento, temperatura de 21±2 °C y fotoperiodo continuo de 24 h.
En el tercer ensayo se analizaron salinidades de 0, 1.5, 3 y 5 % empleando el mismo medio de cultivo, manteniendo 92.59 μmol m-2 s-1, 22±2 °C y agitación continua; posteriormente se evaluó el crecimiento mixotrófico utilizando derivados lácteos por triplicado (suero, leche entera y yogurt al 50 %) comparados con un control autotrófico con Nitrofoska 3 mL/L, con tres repeticiones por tratamiento en cultivos discontinuos alimentados.
El yogurt natural semidescremado empleado como sustrato fue sometido previamente a un proceso de biodegradación aerobia con aireación lenta. Para ello, se prepararon 3 litros de yogurt natural semidescremado al 5 % (v/v) en un envase plástico abierto, con aireación continúa suministrada mediante un compresor de baja presión tipo pecera, sin filtración, esterilización ni pretratamiento adicional. El proceso se llevó a cabo sin control de temperatura ni iluminación adicional. Cada 3 días se tomaron muestras del sustrato para determinar la población de levaduras, bacilos, bacterias y hongos mediante recuento en cámara de Neubauer, con el fin de monitorear la dinámica microbiana del sustrato antes de inocular la microalga, al momento de su uso, el sustrato al 5 % (v/v) presentó un pH de 7; en el cuarto ensayo se evaluaron concentraciones de yogurt natural de 5, 10, 20 y 50 %; los cultivos fueron iniciados con un inóculo de 1×106 cel·mL-1 y un control sin microalga, mantenidos todos a 166.66 μmol m-2 s-1, fotoperiodo de 24 h, temperatura de 22±2 °C y aireación constante.
En relación al 5to ensayo se realizó en frascos de 6 L con 5 L de medio evaluando cultivo autotrófico, cultivo mixotrófico con yogurt al 5 % (v/v).
La densidad celular se determinó cada tres días mediante recuento en cámara de Neubauer hasta alcanzar la fase estacionaria, en los cultivos mixotróficos con yogurt, el recuento incluyó microalgas, levaduras y hongos filamentosos tabicados presentes en el consorcio; la discriminación de Chlorella sp. de estos microorganismos se realizó por criterios morfológicos (tamaño de 3–17 µm, forma esférica-elipsoidal, coloración verde y ausencia de flagelos), la velocidad específica de crecimiento (µ) y el tiempo de duplicación (td) se calcularon según 10. Los pigmentos fotosintéticos se extrajeron a partir de 2 mL de cultivo centrifugado utilizando acetona/metanol (2:1) y se cuantificaron espectrofotométricamente a 665 nm, 649 nm y 480 nm para clorofila a, clorofila b y carotenoides; respectivamente y aplicando las ecuaciones descritas por 11. La biomasa seca se determinó mediante secado de alícuotas de cultivo a 70 °C durante 24 h hasta peso constante, el análisis proximal de la biomasa incluyó determinación de humedad, proteína, grasa, cenizas y fibra mediante métodos INEN 518, 519, 520, 522 y 523; los carbohidratos totales se calcularon por diferencia y el contenido energético se estimó empleando factores de conversión estándar.
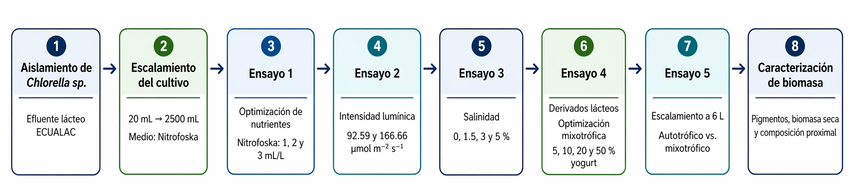
Figura 1. Esquema experimental del proceso de cultivo y caracterización de Chlorella sp.
RESULTADOS
Identificación y caracterización de la microalga
La microalga utilizada en el estudio fue obtenida a partir de un consorcio microalgal previamente empleado en un ensayo de tratabilidad de efluente lácteo, compuesto por Chlamydomonas sp., Chlorella sp., Euglena sp. y levaduras; durante el proceso de mantenimiento y cultivo, se observó el predominio de la cepa Chlorella sp., la cual fue posteriormente aislada para su evaluación experimental.
La identificación taxonómica fue confirmada mediante observación microscópica y validación especializada (comunicación personal, Dra. Gloria Garduño, presidenta de la Sociedad Mexicana de Ficología), las observaciones microscópicas permitieron reconocer las características morfológicas compatibles con el género Chlorella, utilizadas como criterio de confirmación del organismo experimental (Figura 2).
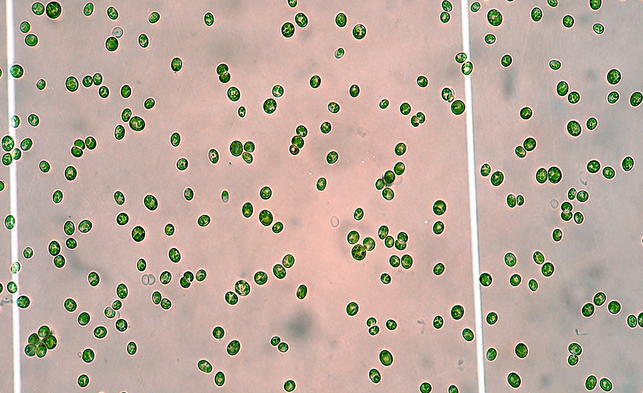
Figura 2. Observación al microscopio de la microalga Chlorella sp.
Efecto de la concentración de fertilizante (Nitrofoska)
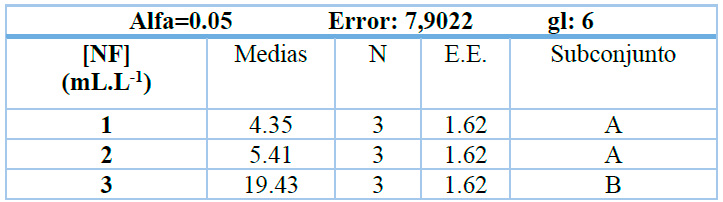
Tabla 1. Prueba de Duncan para la variable densidad celular (cel·mL-1).
Como se muestra en la Tabla 1 el análisis de varianza aplicado a los valores de densidad celular mostró diferencias significativas entre tratamientos (p = 0.0010), la prueba de Duncan evidenció que la concentración de 3 mL·L-1 de fertilizante Nitrofoska promovió el mayor crecimiento celular en comparación con 1 y 2 mL·L-1. La densidad celular máxima alcanzó 26 × 106 cel·mL-1 a 3 mL·L-1; las curvas de crecimiento mostraron el inicio de la fase exponencial a partir del día 3 en todos los tratamientos (Figura 3), los valores máximos de densidad celular para 1 y 2 mL·L-1 se registraron al día 9; mientras que el tratamiento de 3 mL·L-1 alcanzó su máximo al día 12.
Figura 3. Curva de crecimiento (x106 cel·mL-1) en función de la concentración de Nitrofoska (1, 2, 3 mL.L-1).
El tiempo de duplicación durante la fase exponencial fue de 1.870 h para 1 mL·L-1, 2.005 h para 2 mL·L-1 y 2.340 h para 3 mL·L-1 (Tabla 2), lo que indica que la mayor tasa de crecimiento relativa durante la fase exponencial se registró a la menor concentración de fertilizante. Sin embargo, la densidad celular final fue la variable principal utilizada para seleccionar el tratamiento óptimo, por ser el indicador directo del rendimiento total de biomasa al final del cultivo; bajo este criterio, la concentración de 3 mL·L-1 fue seleccionada como óptima al ser el único tratamiento que alcanzó un subconjunto estadísticamente diferente (Tabla 1), a pesar de presentar la menor tasa de crecimiento durante la fase exponencial.
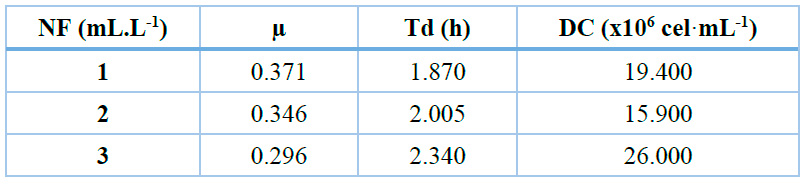
Tabla 2. Velocidades de crecimiento (μ), tiempos de duplicación (Td) y densidad celular máxima (DC) en función de la concentración de Nitrofoska (1, 2, 3 mL·L-1).
Los valores máximos de densidad celular alcanzados a en presencia de 1 y 2 mL·L-1 de Nitrofoska coincidieron al noveno día de haber comenzado el experimento; mientras que con el 3 mL·L-1 de fertilizante, la microalga produjo el máximo crecimiento a los 12 días.
Efecto de la intensidad luminosa
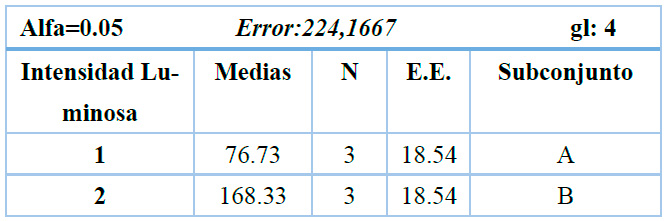
Tabla 3. Ensayo 2. Prueba de Duncan para la variable densidad celular (cel·mL-1).
En la Tabla 3 se presentan los resultados del análisis estadístico, que evidenció diferencias significativas entre las intensidades luminosas evaluadas (p = 0.0250). La intensidad de 166.66 µmol·m-2·s-1 fue seleccionada como condición óptima tomando como variable principal la densidad celular final, por ser el indicador del rendimiento total de biomasa; bajo este criterio, esta intensidad favoreció el crecimiento microalgal en comparación con 92.59 µmol·m-2·s-1; las curvas de crecimiento mostraron el inicio de la fase exponencial desde el día 3 para ambos tratamientos (Figura 4). La mayor intensidad luminosa permitió alcanzar una densidad celular máxima de 808 × 10⁶ cel·mL-1 con un tiempo de duplicación de 1.553 h, mientras que la menor intensidad alcanzó 160 × 10⁶ cel·mL-1 y un Td de 1.639 h (Tabla 4); en este ensayo, la mayor densidad celular final coincidió con la mejor cinética de crecimiento, lo que refuerza la selección de 166.66 µmol·m-2·s-1 como condición óptima. El crecimiento obtenido a mayor intensidad luminosa superó aproximadamente 5.05 veces al registrado bajo menor iluminación, los máximos de crecimiento se alcanzaron al día 15 y día 12; respectivamente.
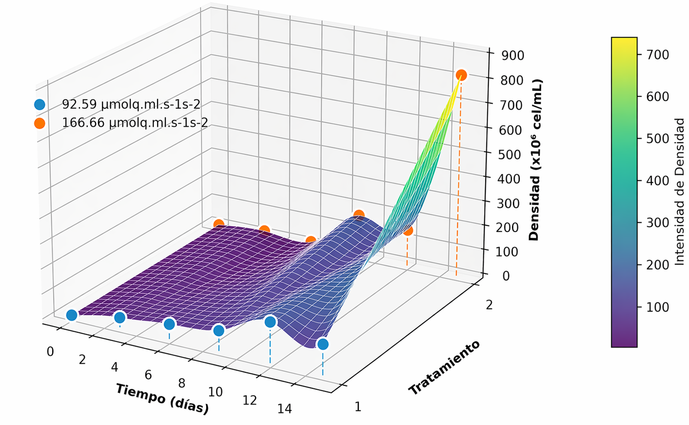
Figura 4. Curvas de crecimiento según intensidad luminosa (µmol·m-2·s-1).
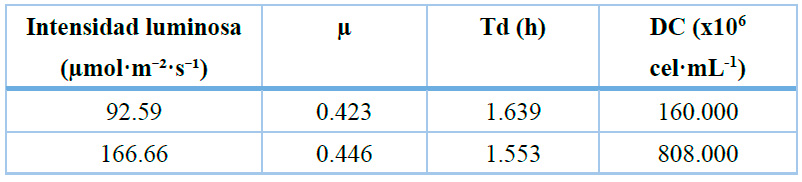
Tabla 4. Parámetros cinéticos de crecimiento.
Efecto de la salinidad
El análisis de varianza indicó que las diferencias entre tratamientos no fueron estadísticamente significativas (p = 0.1161); por lo tanto, no puede afirmarse que ningún tratamiento sea superior a otro con base en este análisis. No obstante, de manera descriptiva, la prueba de Duncan mostró que la salinidad de 1.5 % tendió a presentar valores de densidad celular mayores que los demás tratamientos evaluados (Tabla 5).
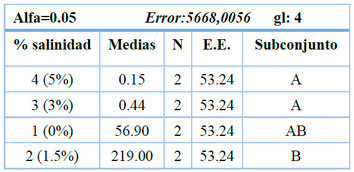
Tabla 5. Ensayo 3. Prueba de Duncan para la variable densidad celular (cel·mL-1).
Las curvas de crecimiento evidenciaron el inicio de la fase exponencial desde el día 3 en los tratamientos evaluados (Figura 5).
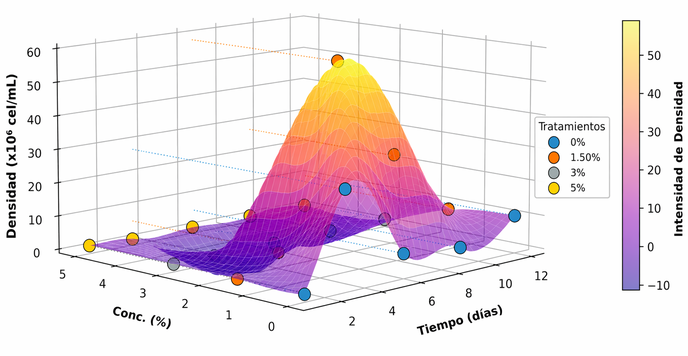
Figura 5. Curvas de crecimiento según salinidad.
A 1.5 % de salinidad se alcanzó la mayor densidad celular final (58 × 106 cel·mL-1), mientras que a 0 % de salinidad se registró la mayor tasa específica de crecimiento (µ = 1.655) y el menor tiempo de duplicación (Td = 0.419 h), con una densidad celular de 27.4 × 106 cel·mL⁻¹ (Tabla 6). Dado que el análisis de varianza no evidenció diferencias estadísticamente significativas entre tratamientos (p = 0.1161), no es posible establecer una salinidad óptima con respaldo estadístico; los valores descritos deben interpretarse de forma exploratoria. La salinidad entre 3 y 5 % produjo un efecto negativo sobre el crecimiento, observándose una disminución marcada de la población celular hasta valores cercanos a 0.150 × 106 cel·mL-1, lo que indica un efecto inhibitorio o letal bajo estas condiciones. Con base en estos resultados, los ensayos posteriores se desarrollaron sin adición de sal (0 %), condición que presentó los mejores parámetros cinéticos y que garantiza la ausencia de estrés osmótico sobre el cultivo.
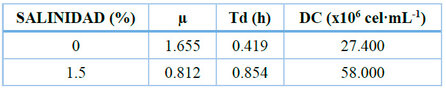
Tabla 6. Parámetros cinéticos de crecimiento.
Evaluación de derivados lácteos como fuente orgánica
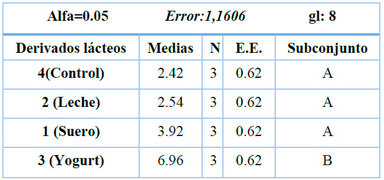
Tabla 7. Prueba de Duncan para derivados lácteos.
La tabla 7 muestra que en el análisis de varianza hay diferencias significativas en la densidad celular entre los derivados lácteos evaluados (p < 0.05); la prueba de Duncan mostró que el yogurt natural semidescremado promovió el mayor crecimiento en comparación con suero y leche, las curvas de crecimiento indicaron que el cultivo con yogurt presentó una fase exponencial más prolongada y una mayor densidad celular final (Figura 6). El tratamiento con suero mostró crecimiento intermedio, mientras que la leche registró los valores más bajos de densidad celular.
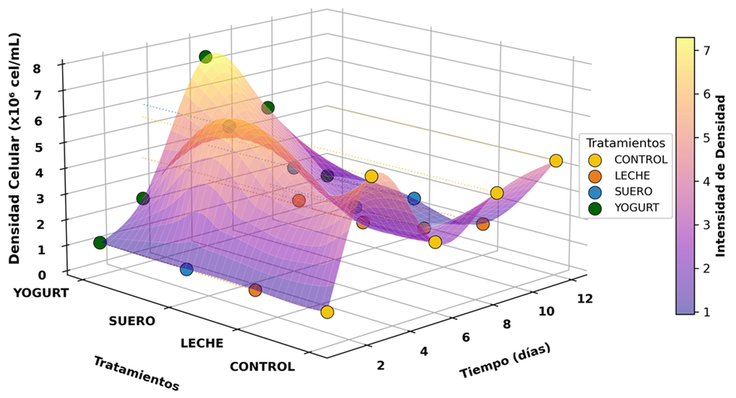
Figura 6. Curvas de crecimiento con diferentes derivados lácteos.
Los parámetros cinéticos mostraron que el suero presentó la mayor tasa específica de crecimiento (µ = 0.903) y el menor tiempo de duplicación (Td = 0.768 h), seguido por el control autotrófico (µ = 0.854, Td = 0.811 h); sin embargo, el yogurt alcanzó la mayor densidad celular final (7.330 × 106 cel·mL-1), que fue la variable principal utilizada para la selección del derivado lácteo, por representar el rendimiento total de biomasa al final del cultivo (Tabla 8). Con base en este criterio, el yogurt natural semidescremado fue seleccionado como el sustrato orgánico más adecuado para los ensayos de optimización posteriores.
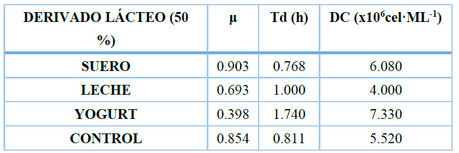
Tabla 8. Parámetros cinéticos de crecimiento.
Optimización del cultivo mixotrófico con yogurt
El análisis de varianza mostró diferencias significativas entre las concentraciones de yogurt evaluadas (p < 0.05); la prueba de Duncan indicó que las concentraciones de 5 % y 10 % (v/v) fueron estadísticamente superiores al 50 %, ubicándose ambas en el subconjunto B, sin diferir significativamente entre sí (Tabla 9). La concentración de 20 % también perteneció al subconjunto B, por lo que las tres concentraciones intermedias no difirieron estadísticamente entre sí.
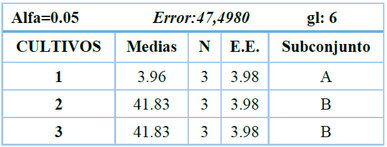
Tabla 9. Prueba de Duncan para la variable densidad celular (cel·mL-1).
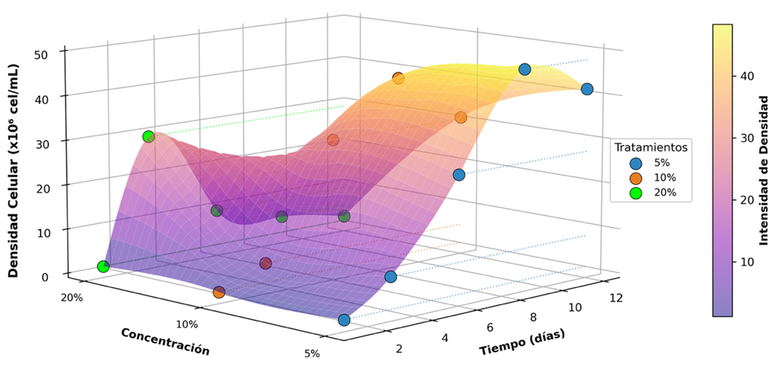
Figura 7. Curva de crecimiento (x106 cel·mL-1) de la microalga Chlorella sp. con derivado lácteo yogurt natural semidescremado a diferentes concentraciones (5,10, 20 %).
En la Figura 7 se muestra las curvas de crecimiento evidenciaron incremento sostenido en todos los tratamientos, aunque con variaciones en la duración de la fase exponencial; la densidad celular máxima se registró en la concentración óptima seleccionada, mientras que concentraciones superiores no produjeron incrementos proporcionales, los parámetros cinéticos mostraron diferencias en el tiempo de duplicación, con el menor Td asociado a dicha concentración (Tabla 10).
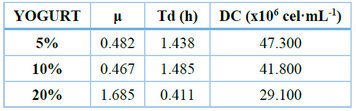
Tabla 10. Velocidades de crecimiento (μ), tiempos de duplicación (Td) y densidad celular máxima (DC) en función del derivado lácteo yogurt a diferentes concentraciones (5%,10 % y 20 %).
Con base en estos resultados, se seleccionó la concentración de 5 % (v/v) como la más adecuada para la comparación con el cultivo autotrófico, criterio sustentado en que alcanzó la mayor densidad celular final (47.3×106 cel·mL-1), a pesar de que la concentración de 20 % presentó la mayor tasa específica de crecimiento (µ = 1.685) y el menor tiempo de duplicación (Td = 0.411 h). La densidad celular máxima final fue el parámetro prioritario de selección por representar el rendimiento total de biomasa al final del cultivo. En la comparación directa entre el sistema mixotrófico al 5 % y el cultivo autotrófico, el análisis de varianza no mostró diferencias estadísticamente significativas (p = 0.3716); la prueba de Duncan ubicó ambos tratamientos en el mismo subconjunto (Tabla 11). En términos descriptivos, el cultivo mixotrófico presentó una tendencia hacia mayor densidad celular media (28.03 × 10⁶ vs. 22.97 × 106 cel·mL-1), aunque esta diferencia no fue estadísticamente sustentada.
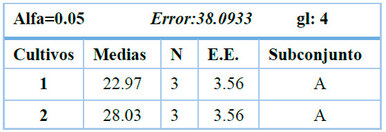
Tabla 11. Prueba de Duncan para la variable densidad celular (cel·mL-1).
Caracterización de pigmentos
El contenido de clorofila total no presentó diferencias estadísticamente significativas entre tratamientos al día 15 (p = 0.6463), por lo que no puede afirmarse que ningún sistema produjo mayor acumulación de pigmentos en esa fecha.
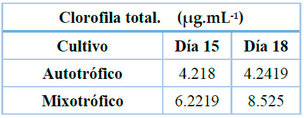
Tabla 12. Contenido de clorofila total.
Composición proximal de la biomasa
El análisis proximal evidenció variaciones en el contenido de proteína, lípidos, carbohidratos y cenizas entre los sistemas de cultivo evaluados (Tabla 13).
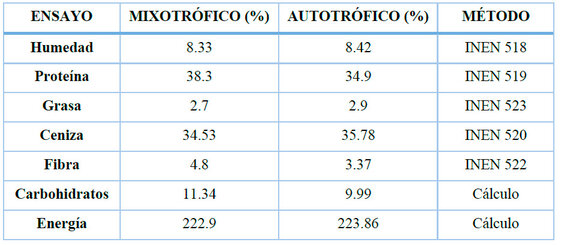
Tabla 13. Análisis proximal de los cultivos mixotrófico y autotrófico.
El contenido de proteína representó la fracción mayoritaria de la biomasa en ambos tratamientos, los lípidos y carbohidratos mostraron diferencias porcentuales entre el cultivo autotrófico y el mixotrófico. El contenido de cenizas presentó valores comparables entre tratamientos; los valores reportados en la Tabla 13 corresponden a determinaciones individuales por tratamiento y no fueron sometidos a análisis estadístico comparativo, por lo que las diferencias observadas entre cultivos deben interpretarse de forma descriptiva y no pueden atribuirse conclusivamente al tipo de cultivo.
Composición mineral y evaluación económica
La concentración de azufre y otros elementos minerales mostró variaciones entre tratamientos (Tabla 14), el cultivo suplementado presentó incremento relativo en algunos elementos respecto al control; el análisis de metales pesados indicó concentraciones dentro de los rangos evaluados experimentalmente (Tabla 14).
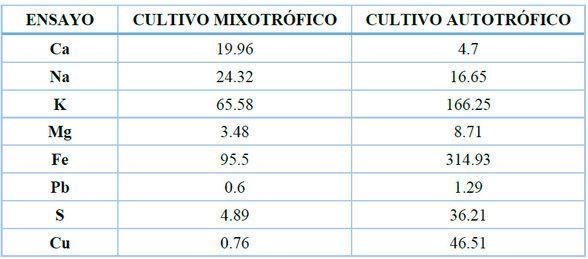
Tabla 14. Contenido de metales y de azufre (%) en la biomasa de Chlorella sp. en cultivos mixotróficos y autotróficos.
El análisis económico consideró exclusivamente el costo del medio de cultivo como insumo principal, sin incluir costos de electricidad, agua destilada, equipamiento ni mano de obra; los valores reportados corresponden por tanto a una estimación parcial del costo de producción a escala de laboratorio. El fertilizante Nitrofoska Foliar fue adquirido a un precio de referencia de 6.20 USD·L-1 de producto; aplicado a la dosis de 3 mL·L-1 de cultivo, el costo por litro de cultivo resultó en 0.0186 USD·L-1 (Tabla 15), la productividad de biomasa seca del sistema autotrófico fue de 0.815 g·L-1 (38.32 g obtenidos en 47.0 L de cultivo); por lo tanto, producir 1 g de biomasa seca requiere 1.227 L de cultivo y 3.7 mL de Nitrofoska, con un costo de 0.023 USD·g-1 de biomasa seca, reportado como 0.03 USD·g-1 por redondeo en la Tabla 16; el yogurt natural semidescremado fue adquirido a un precio de referencia de 2.60 USD·L-1; aplicado a la dosis de 50 mL·L-1 de cultivo (5 % v/v), el costo por litro de cultivo fue de 0.13 USD·L⁻¹ (Tabla 15), la productividad de biomasa seca del sistema mixotrófico fue de 3.169 g·L-1 (72.89 g obtenidos en 23.0 L de cultivo); por lo tanto, producir 1 g de biomasa seca requiere 0.316 L de cultivo y 15.82 mL de yogurt, con un costo de 0.04 USD·g-1 de biomasa seca (Tabla 16). La diferencia entre ambos costos es de 0.017 USD·g-1, por lo que en términos del costo del medio de cultivo ambos sistemas presentan una estructura comparable a escala de laboratorio.
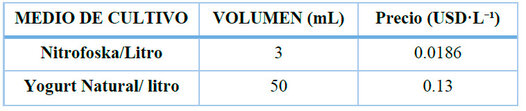
Tabla 15. Análisis de costos de Medios de cultivo utilizados en un litro de agua destilada.
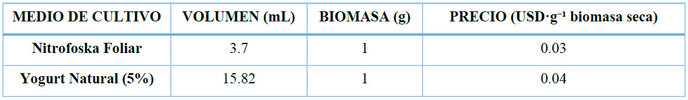
Tabla 16. Costos para producir 1g (gramo) de biomasa seca con cultivo autotrófico (Fertilizante Foliar Nitrofoska) y cultivo mixotrófico (yogurt natural semidescremado).
DISCUSIÓN
La respuesta de Chlorella sp. bajo condiciones autotróficas evidenció que el crecimiento estuvo condicionado por la disponibilidad de nutrientes, la intensidad luminosa y la salinidad del medio como lo menciona 12; la concentración intermedia del fertilizante comercial permitió alcanzar mayores densidades celulares y menores tiempos de duplicación, lo que indica que un balance adecuado de nitrógeno y fósforo favorece la división celular sin generar efectos inhibitorios asociados a concentraciones elevadas 13.
En microalgas verdes se ha reportado que el exceso de nutrientes puede alterar la relación N:P y modificar la eficiencia metabólica, afectando la cinética de crecimiento 14. Resultados similares en especies del género Chlorella muestran que concentraciones moderadas de fertilización promueven mayor productividad en comparación con niveles extremos, donde se observan limitaciones fisiológicas o acumulación de compuestos no estructurales 15.
En relación con la intensidad luminosa, el incremento del crecimiento hasta un umbral determinado confirma el comportamiento típico de saturación fotosintética descrito para microalgas clorofíceas, cuando la radiación supera la capacidad de procesamiento del aparato fotosintético, la eficiencia cuántica disminuye y pueden activarse mecanismos de disipación de energía para evitar daño fotooxidativo16, 17.
La fase exponencial más prolongada bajo intensidades moderadas sugiere que la microalga mantiene una relación estable entre captación de luz y fijación de carbono, condición que ha sido señalada como determinante para maximizar la productividad en sistemas autotróficos controlados 18.
Respecto a la salinidad, los resultados mostraron de forma descriptiva una reducción en la densidad celular a concentraciones de 3 y 5 %, lo que podría indicar un efecto inhibitorio a niveles elevados de NaCl. Este comportamiento es consistente con lo descrito en la literatura para especies del género Chlorella, donde el aumento de la salinidad puede asociarse a un mayor costo energético por osmorregulación y a una posible reducción de la eficiencia fotosintética 19. Sin embargo, dado que el análisis de varianza no mostró diferencias estadísticamente significativas entre tratamientos (p = 0.1161), estas observaciones deben considerarse exploratorias y no permiten establecer con certeza estadística un rango de salinidad óptimo ni afirmar que algún nivel produjo un rendimiento superior a otro 20. Los patrones observados son consistentes con tendencias reportadas en la literatura, aunque su confirmación requeriría un diseño experimental con mayor poder estadístico19. En especies del género Chlorella se ha descrito que el aumento de la salinidad puede disminuir la eficiencia fotosintética y redirigir el metabolismo hacia procesos de adaptación osmótica, lo que reduce la productividad global 20,21.
El crecimiento de Chlorella sp. en presencia de derivados lácteos evidenció una respuesta diferenciada respecto al sistema estrictamente autotrófico, lo que podría estar relacionado con la disponibilidad simultánea de carbono orgánico y energía luminosa, aunque los mecanismos específicos de adaptación metabólica no fueron evaluados directamente en este estudio 22.
En Chlorella también se ha descrito en la literatura que la disponibilidad de fuentes orgánicas fácilmente metabolizables puede acelerar la tasa específica de crecimiento a través de rutas glicolíticas y del ciclo de los ácidos tricarboxílicos; sin embargo, la integración metabólica de las fuentes de carbono no fue medida directamente en este trabajo, por lo que esta interpretación debe considerarse como una hipótesis plausible 23.
Entre los sustratos evaluados, el yogurt natural semidescremado mostró un efecto más consistente en la cinética de crecimiento, especialmente a concentraciones intermedias. Este comportamiento puede asociarse no solo al aporte de lactosa y otros compuestos orgánicos, sino también a la posible presencia de metabolitos derivados de la fermentación láctica que podrían facilitar la disponibilidad de carbono reducido en el medio 24.
Estudios previos han señalado que en cultivos mixotróficos la concentración del sustrato orgánico debe mantenerse dentro de un rango óptimo, ya que niveles elevados pueden generar inhibición por sobrecarga metabólica o alteraciones en el equilibrio osmótico 25,26. La ausencia de incrementos proporcionales a mayores concentraciones observada en este estudio sigue esa tendencia, lo que indica que el beneficio del sistema mixotrófico depende de un ajuste fino entre aporte orgánico y capacidad metabólica celular 27.
La comparación entre el cultivo mixotrófico suplementado al 5 % (v/v) y el sistema autotrófico control mostró, en términos descriptivos, una tendencia hacia mayor densidad celular media en el tratamiento suplementado; sin embargo, el análisis estadístico no evidenció diferencias significativas entre ambos sistemas (p = 0.3716, Tabla 11). Este resultado no permite afirmar que la combinación de fotosíntesis y asimilación heterotrófica produjo una sinergia metabólica demostrable en las condiciones evaluadas, aunque la tendencia observada es consistente con lo descrito en la literatura para sistemas mixotróficos 28. Además, la ausencia de alteraciones morfológicas observadas al microscopio indica que el suplemento no generó efectos visibles de estrés celular, lo que refuerza la viabilidad fisiológica del sistema evaluado.
Estos resultados son consistentes con la idea de que residuos o subproductos agroindustriales podrían integrarse como fuentes complementarias de carbono en sistemas de producción microalgal; no obstante, la viabilidad de esta estrategia depende del control de concentraciones y condiciones ambientales del cultivo, aspectos que requieren evaluación adicional antes de extrapolar conclusiones 29. La utilización de derivados lácteos como suplemento no solo influye en la cinética de crecimiento, sino que también abre la posibilidad de vincular procesos de valorización de residuos con la producción de biomasa microalgal 30. Sin embargo, la estabilidad del sistema a mayor escala y su impacto en la composición bioquímica de la biomasa requieren análisis adicionales para confirmar su aplicabilidad en escenarios productivos más amplios.
La comparación integral entre el sistema autotrófico y el cultivo mixotrófico suplementado permitió observar variaciones descriptivas en la densidad celular máxima, el tiempo de duplicación y la acumulación de biomasa. Dado que el análisis estadístico no evidenció diferencias significativas en densidad celular (p = 0.3716, Tabla 11), ninguna de las variables comparadas entre sistemas puede interpretarse como evidencia concluyente de superioridad del cultivo mixotrófico. Los valores de productividad de biomasa registrados (3.16 g·L-1 en mixotrofía vs. 0.81 g·L-1 en autotrofía) corresponden a determinaciones descriptivas del ensayo de escalamiento y no fueron sometidos a análisis estadístico comparativo; su diferencia numérica es consistente con tendencias reportadas en la literatura para sistemas mixotróficos 31, pero no puede atribuirse conclusivamente a una ventaja del sistema bajo las condiciones evaluadas. En este contexto, los mecanismos metabólicos subyacentes tampoco fueron medidos directamente en este trabajo, por lo que cualquier interpretación mecanística debe considerarse especulativa 31.
El análisis de pigmentos mostró que las condiciones de cultivo se asociaron con diferencias descriptivas en la concentración de compuestos liposolubles; sin embargo, dado que el análisis estadístico de clorofila total al día 15 no mostró diferencias significativas (p = 0.6463), las variaciones observadas deben interpretarse con cautela y no pueden atribuirse conclusivamente al tipo de cultivo 32. En sistemas mixotróficos, la menor dependencia exclusiva de la fotosíntesis puede modificar la proporción de clorofilas y carotenoides, dependiendo del equilibrio entre respiración y fijación de carbono 33. Cambios en la composición pigmentaria han sido asociados tanto a respuestas adaptativas frente a variaciones ambientales como a estrategias de optimización energética; lo que sugiere que las diferencias observadas no solo reflejan crecimiento acelerado, sino también ajustes fisiológicos más amplios 34.
En cuanto a la composición proximal de la biomasa, las variaciones registradas entre sistemas indican que el tipo de cultivo puede incidir en la proporción de proteínas, lípidos y otros componentes estructurales. En este estudio, las diferencias en composición proximal entre cultivos fueron pequeñas (Tabla 13), lo que sugiere que el suplemento lácteo no modificó sustancialmente la calidad bromatológica de la biomasa bajo las condiciones evaluadas. Se ha descrito que la disponibilidad de carbono orgánico en cultivos mixotróficos puede favorecer la acumulación de biomasa total, aunque la fracción proteica y lipídica puede variar según la fuente y concentración del sustrato 35,36.
En este estudio, las diferencias en composición proximal entre cultivos fueron pequeñas y no permiten concluir que el suplemento lácteo modificó la calidad nutricional de la biomasa; para determinar si existe un impacto en aplicaciones alimentarias o biotecnológicas se requieren análisis más detallados de perfil de aminoácidos, ácidos grasos y biodisponibilidad 37.
Desde una perspectiva productiva, el sistema mixotrófico evaluado mostró, a escala de laboratorio, mayor productividad de biomasa en términos descriptivos; no obstante, dado que la comparación estadística directa de densidad celular no fue significativa (p = 0.3716), las ventajas del sistema mixotrófico sobre el autotrófico no pueden afirmarse de forma concluyente con los datos disponibles. Su implementación a mayor escala requeriría además considerar la estabilidad del cultivo, el control microbiológico y la reproducibilidad del sustrato utilizado38. La incorporación de derivados lácteos como fuente complementaria de carbono representa una línea de investigación de interés para la valorización de subproductos agroindustriales, aunque su viabilidad a escala mayor dependerá del balance entre costos, disponibilidad del insumo, control microbiológico y consistencia en la composición de la biomasa obtenida 39. En este sentido, los resultados obtenidos aportan evidencia experimental sobre el potencial del sistema evaluado, pero también indican la necesidad de estudios adicionales orientados a optimizar parámetros operativos y evaluar el desempeño en condiciones de producción más amplias 40.
En términos generales, la respuesta observada en Chlorella sp. bajo el esquema evaluado es consistente con la idea de que la optimización de sistemas de cultivo microalgal requiere considerar la interacción entre fuente de carbono, disponibilidad energética y condiciones fisicoquímicas del medio. Diversos estudios han señalado que la transición de sistemas autotróficos a esquemas mixotróficos puede incrementar la productividad, aunque también puede modificar la dinámica metabólica y la composición de la biomasa 41. En este estudio, la tendencia descriptiva hacia mayor productividad de biomasa bajo suplementación orgánica es consistente con ese patrón descrito en la literatura; no obstante, dado que las diferencias estadísticas en densidad celular no fueron significativas, no puede afirmarse que la cepa evaluada demostró flexibilidad metabólica. La ausencia de alteraciones morfológicas observables indica que el suplemento no generó efectos de estrés visibles a nivel celular 42.
La incorporación de derivados lácteos como fuente complementaria de carbono se relaciona con estrategias actuales de valorización de residuos agroindustriales en bioprocesos microalgales; se ha propuesto que el uso de subproductos orgánicos puede disminuir costos asociados a medios sintéticos, aunque su impacto depende de la composición del residuo, la necesidad de tratamientos previos y el control microbiológico del sistema 43,44. Asimismo, las variaciones observadas en la composición proximal y pigmentaria deben interpretarse considerando que en sistemas mixotróficos el flujo de carbono puede redistribuirse hacia diferentes rutas biosintéticas; lo cual influye en la proporción relativa de proteínas, lípidos y compuestos fotosintéticos 45. Estudios previos han indicado que la disponibilidad de carbono orgánico puede favorecer la acumulación de biomasa total sin que necesariamente se mantenga constante la fracción proteica o lipídica 46. En ese sentido, las variaciones descriptivas registradas en la composición de la biomasa deben analizarse con mayor profundidad en estudios futuros, dado que en este trabajo no fueron sometidas a análisis estadístico comparativo.
CONCLUSIONES
En un marco más amplio, estos resultados se integran en la discusión actual sobre intensificación de cultivos microalgales mediante estrategias híbridas que combinen fotosíntesis y asimilación heterotrófica. Si bien el sistema evaluado mostró ventajas en términos cinéticos, la literatura advierte que factores como estabilidad del cultivo, competencia microbiana y control de parámetros ambientales pueden condicionar el desempeño a mayor escala 47. Por ello, el análisis del presente estudio debe entenderse como una aproximación experimental al uso de suplementos lácteos en cultivo de Chlorella sp., cuya validación en condiciones operativas más amplias requerirá evaluaciones adicionales.
Se demostró que el crecimiento de Chlorella sp. está condicionado por la interacción entre disponibilidad de nutrientes, intensidad luminosa y salinidad; los resultados autotróficos permitieron definir una línea base fisiológica del cultivo, la suplementación con derivados lácteos modificó descriptivamente la cinética de crecimiento bajo condiciones mixotróficas, particularmente a concentraciones intermedias de yogurt natural semidescremado; no obstante, la comparación directa entre el sistema mixotrófico al 5 % (v/v) y el cultivo autotrófico no evidenció diferencias estadísticamente significativas en densidad celular (p = 0.3716, Tabla 11), por lo que no puede afirmarse que el sistema mixotrófico produjo un rendimiento celular superior; las diferencias descriptivas observadas en tiempo de duplicación, composición proximal y pigmentos no fueron respaldadas por análisis estadístico comparativo y deben interpretarse con cautela.
Se registraron variaciones descriptivas en la composición proximal y pigmentaria de la biomasa entre sistemas de cultivo; en conjunto, los resultados indican que la integración controlada de un suplemento lácteo puede constituir una estrategia potencial para la producción de biomasa microalgal bajo condiciones de laboratorio, aunque las ventajas del sistema mixotrófico sobre el autotrófico no pueden afirmarse de forma concluyente con los datos disponibles, no obstante, la comparación estadística directa entre cultivo autotrófico y mixotrófico no evidenció diferencias significativas en densidad celular (Tabla 11), por lo que las afirmaciones sobre superioridad del sistema mixotrófico deben interpretarse con cautela. La validación de esta estrategia a escala productiva requiere estudios adicionales que evalúen la estabilidad del cultivo, el control microbiológico y la reproducibilidad del sistema.
Materiales suplementarios: No hay materiales suplementarios disponibles para este artículo.
Contribuciones de los autores: Geovanna Elizabeth Guevara Figueroa y Pedro José Rachid Romero Saker contribuyeron sustancialmente al trabajo experimental, la adquisición de datos, el análisis formal y la redacción del borrador original. Ever Darío Morales Avendaño contribuyó a la conceptualización, la supervisión del estudio, la administración del proyecto, la financiación y la revisión crítica del manuscrito. Junior Jesús Vélez Espinoza contribuyó a la conceptualización, la curación de datos, la revisión y edición del manuscrito. Todos los autores contribuyeron a la interpretación de los resultados, revisaron críticamente el manuscrito, aprobaron la versión final y aceptan responsabilidad por todos los aspectos del trabajo.
Financiación: Esta investigación fue financiada por Ever Darío Morales Avendaño. No se recibió financiación externa.
Declaración del comité de ética / revisión institucional: Este estudio no involucró participantes humanos, animales ni registros clínicos. Por tanto, no requirió aprobación por un comité de ética ni evaluación por una junta de revisión institucional, al tratarse de una investigación experimental de laboratorio.
Declaración de consentimiento informado: No aplica.
Disponibilidad de los datos: Los datos que respaldan los hallazgos de este estudio están disponibles a solicitud razonable al autor de correspondencia.
Agradecimientos: Los autores agradecen las facilidades de laboratorio y el apoyo técnico brindado durante la fase experimental del estudio, así como el respaldo institucional que hizo posible el cultivo, seguimiento y caracterización de la biomasa microalgal.
Conflictos de interés: Los autores declaran no tener conflictos de interés.
Declaración sobre el uso de herramientas de inteligencia artificial: La herramienta de inteligencia artificial GPAI (https://gpai.app/) se utilizó exclusivamente para generar el resumen gráfico incluido en este estudio. No se empleó ningún sistema de inteligencia artificial para generar, manipular o analizar los datos experimentales ni los resultados estadísticos. Los autores verificaron de forma independiente todos los resultados, análisis y conclusiones, en cumplimiento de la política de BioNatura Journal sobre inteligencia artificial: https://bionaturajournal.com/artificial-intelligence--ai-.html.
REFERENCES
1. Oslan SNH, Shoparwe NF, Yusoff AH, et al. A Review on Haematococcus pluvialis Bioprocess Optimization of Green and Red Stage Culture Conditions for the Production of Natural Astaxanthin. Biomolecules. 2021;11(2):256. doi:10.3390/biom11020256
2. Salbitani G, Carfagna S. Ammonium Utilization in Microalgae: A Sustainable Method for Wastewater Treatment. Sustainability. 2021;13(2):956. doi:10.3390/su13020956
3. Pereira L, Cotas J, Valado A. Antioxidants from microalgae and their potential impact on human well-being. Explor Drug Sci. 2024;2(3):292-321. doi:10.37349/eds.2024.00048
4. Capeletti L, Mossi A, Treichel H. EXTRACTION OF BIOPRODUCTS FROM MICROALGAE: A REVIEW OF METHODOLOGIES AND SCALE-UP STRATEGIES. Rev Multidiscip Nordeste Min. 2025;19:1-32. doi:10.61164/sgdfdc52
5. Paterson S, Gómez-Cortés P, de la Fuente MA, Hernández-Ledesma B. Bioactivity and Digestibility of Microalgae Tetraselmis sp. and Nannochloropsis sp. as Basis of Their Potential as Novel Functional Foods. Nutrients. 2023;15(2):477. doi:10.3390/nu15020477
6. Escobedo MJ, Calderón AC, Escobedo MJ, Calderón AC. Biomasa microalgal con alto potencial para la producción de biocombustibles. Sci Agropecu. 2021;12(2):265-282. doi:10.17268/sci.agropecu.2021.030
7. Szotkowski M, Holub J, Šimanský S, et al. Bioreactor Co-Cultivation of High Lipid and Carotenoid Producing Yeast Rhodotorula kratochvilovae and Several Microalgae under Stress. Microorganisms. 2021;9(6):1160. doi:10.3390/microorganisms9061160
8. Je S, Yamaoka Y. Biotechnological Approaches for Biomass and Lipid Production Using Microalgae Chlorella and Its Future Perspectives. 2022;32(11):1357-1372. doi:10.4014/jmb.2209.09012
9. González LM, Bashan LE. Toward the Enhancement of Microalgal Metabolite Production through Microalgae–Bacteria Consortia. Biology. 2021;10(4):282. doi:10.3390/biology10040282
10. López Arias T, Galeano E, Santos M, Rodríguez Bonet S, Benitez A. Cinética de crecimiento y productividad lipídica del alga Tetradesmus wisconsinensis S. obtenida en un cuerpo de agua de Paraguay. Investig Agrar. 2016;18:22-29. doi:10.18004/investig.agrar.2016.junio.22-29
11. Sartory DP. The determination of algal chlorophyllous pigments by high performance liquid chromatography and spectrophotometry. Water Res. 1985;19(5):605-610. doi:10.1016/0043-1354(85)90066-1
12. Montoya C, Guzmán Duque FL, Quintero Díaz JC. Biomass and lipid production by the native green microalgae Chlorella sorokiniana in response to nutrients, light intensity, and carbon dioxide: experimental and modeling approach. Front Bioeng Biotechnol. 2023;11. doi:10.3389/fbioe.2023.1149762
13. Michael A, Mtaki K. Optimizing Growth Conditions and Biomass Accumulation for Chlorella vulgaris of the Western Indian Ocean, Tanzania. Int J Biol Chem Sci. 2024;18(6):2066-2077. doi:10.4314/ijbcs.v18i6.1
14. Yaakob MA, Mohamed RMSR, Al-Gheethi A, Gokare RA, Ambati RR. Influence of Nitrogen and Phosphorus on Microalgal Growth, Biomass, Lipid, and Fatty Acid Production: An Overview. Cells. 2021;10(2). doi:10.3390/cells10020393
15. Takahashi M, Karitani Y, Yamada R, Matsumoto T, Ogino H. Co-utilization of microalgae and heterotrophic microorganisms improves wastewater treatment efficiency. Appl Microbiol Biotechnol. 2024;108(1):468. doi:10.1007/s00253-024-13309-w
16. Mazzocchi E, Usai G, Agostino V, et al. Combination of Exhaust Gas Fermentation Effluent and Dairy Wastewater for Microalgae Production: Effect on Growth and FAME Composition of Chlorella sorokiniana. Microorganisms. 2025;13(5):961. doi:10.3390/microorganisms13050961
17. Thepsuthammarat K, Reungsang A, Plangklang P. Microalga Coelastrella sp. Cultivation on Unhydrolyzed Molasses-Based Medium towards the Optimization of Conditions for Growth and Biomass Production under Mixotrophic Cultivation. Molecules. 2023;28(8):3603. doi:10.3390/molecules28083603
18. Mountourakis F, Papazi A, Maragkoudakis A, Stamatis N, Kotzabasis K. Evidencia de adaptación fisiológica de Chlorella vulgaris bajo salinidad extrema: nuevos conocimientos sobre una posible estrategia de halotolerancia. Environ Exp Bot. 2023;216:105543. doi:10.1016/j.envexpbot.2023.105543
19. Yamaoka Y, Petroutsos D, Je S, Yamano T, Li-Beisson Y. Luz, CO2 y almacenamiento de carbono en microalgas. Curr Opin Plant Biol. 2025;84:102696. doi:10.1016/j.pbi.2025.102696
20. Gao P, Guo L, Gao M, Zhao Y, Jin C, She Z. Regulation of carbon source metabolism in mixotrophic microalgae cultivation in response to light intensity variation. J Environ Manage. 2022;302:114095. doi:10.1016/j.jenvman.2021.114095
21. Farooq W. Maximizing Energy Content and CO2 Bio-fixation Efficiency of an Indigenous Isolated Microalga Parachlorella kessleri HY-6 Through Nutrient Optimization and Water Recycling During Cultivation. Front Bioeng Biotechnol. 2022;9. doi:10.3389/fbioe.2021.804608
22. Mazzocchi E, Usai G, Agostino V, et al. Combination of Exhaust Gas Fermentation Effluent and Dairy Wastewater for Microalgae Production: Effect on Growth and FAME Composition of Chlorella sorokiniana. Microorganisms. 2025;13(5). doi:10.3390/microorganisms13050961
23. Chai S, Shi J, Huang T, et al. Characterization of Chlorella sorokiniana growth properties in monosaccharide-supplemented batch culture. PLOS ONE. 2018;13(7):e0199873. doi:10.1371/journal.pone.0199873
24. Amaro HM, Salgado EM, Nunes OC, Pires JCM, Esteves AF. Microalgae systems - environmental agents for wastewater treatment and further potential biomass valorisation. J Environ Manage. 2023;337:117678. doi:10.1016/j.jenvman.2023.117678
25. Gómez L, Tormos-Cedeño L, Ortega-Díaz Y, Gómez-Luna L, Tormos-Cedeño L, Ortega-Díaz Y. Cultivo y aplicaciones de Chlorella vulgaris: principales tendencias y potencialidades en la agricultura. Tecnol Quím. 2022;42(1):70-93.
26. González JF, Cuello TB, Calderón AJ, Calderón M, González J, Carmona D. Cultivation of Autochthonous Microalgae for Biomass Feedstock: Growth Curves and Biomass Characterization for Their Use in Biorefinery Products. Energies. 2021;14(15):4567. doi:10.3390/en14154567
27. Pang N, Gu X, Chen S, Kirchhoff H, Lei H, Roje S. Exploiting mixotrophy for improving productivities of biomass and co-products of microalgae. Renew Sustain Energy Rev. 2019;112:450-460. doi:10.1016/j.rser.2019.06.001
28. Patel AK, Joun J, Sim SJ. A sustainable mixotrophic microalgae cultivation from dairy wastes for carbon credit, bioremediation and lucrative biofuels. Bioresour Technol. 2020;313:123681. doi:10.1016/j.biortech.2020.123681
29. Salinas M, Calatrava-Arrizabalaga P, Ciardi M, Villaró-Cos S, Lafarga T. Development and reutilisation of a fertiliser-based culture medium for the commercial production of Chlorella sorokiniana. Sci Rep. 2025;15(1):23891. doi:10.1038/s41598-025-08320-8
30. Arashiro LT, Josa I, Ferrer I, Van Hulle SWH, Rousseau DPL, Garfí M. Life cycle assessment of microalgae systems for wastewater treatment and bioproducts recovery: Natural pigments, biofertilizer and biogas. Sci Total Environ. 2022;847:157615. doi:10.1016/j.scitotenv.2022.157615
31. Abreu AP, Morais RC, Teixeira JA, Nunes J. A comparison between microalgal autotrophic growth and metabolite accumulation with heterotrophic, mixotrophic and photoheterotrophic cultivation modes. Renew Sustain Energy Rev. 2022;159:112247. doi:10.1016/j.rser.2022.112247
32. Yan X, Shan S, Li X, et al. Carbon and energy metabolism for the mixotrophic culture of Chlorella vulgaris using sodium acetate as a carbon source. Front Microbiol. 2024;15. doi:10.3389/fmicb.2024.1436264
33. Khoobkar Z, Delavari Amrei H. Efecto de las condiciones fototróficas, heterotróficas y mixotróficas sobre el crecimiento y la composición de Anabaena variabilis : Un enfoque de Energy Nexus. Energy Nexus. 2021;2:100010. doi:10.1016/j.nexus.2021.100010
34. Ge S, Qiu S, Tremblay D, Viner K, Champagne P, Jessop PG. Centrate wastewater treatment with Chlorella vulgaris: Simultaneous enhancement of nutrient removal, biomass and lipid production. Chem Eng J. 2018;342:310-320. doi:10.1016/j.cej.2018.02.058
35. Cai Y, Zhai L, Fang X, et al. Effects of C/N ratio on the growth and protein accumulation of heterotrophic Chlorella sp. in broken rice hydrolysate. Biotechnol Biofuels Bioprod. 2022;15(1):102. doi:10.1186/s13068-022-02204-z
36. Yun HS, Kim YS, Yoon HS. Effect of Different Cultivation Modes (Photoautotrophic, Mixotrophic, and Heterotrophic) on the Growth of Chlorella sp. and Biocompositions. Front Bioeng Biotechnol. 2021;9. doi:10.3389/fbioe.2021.774143
37. Xu Q, Hou G, Chen J, et al. Heterotrophically Ultrahigh-Cell-Density Cultivation of a High Protein-Yielding Unicellular Alga Chlorella sp. With a Novel Nitrogen-Supply Strategy. Front Bioeng Biotechnol. 2021;9. doi:10.3389/fbioe.2021.774854
38. Hajri AK, Alsharif I, Albalawi MA, Alshareef SA, Albalawi RK, Jamoussi B. Utilizing Mixed Cultures of Microalgae to Up-Cycle and Remove Nutrients from Dairy Wastewater. Biology. 2024;13(8):591. doi:10.3390/biology13080591
39. Akhmedkhanova R, Dzhambulatov Z, Gadzhaeva Z, Shabanov G, Alieva S. The influence of Chlorella suspension on the quality of milk and its processing products. E3S Web Conf. 2020;222:02021. doi:10.1051/e3sconf/202022202021
40. Abate R, Oon YS, Oon YL, Bi Y. Microalgae-bacteria nexus for environmental remediation and renewable energy resources: Advances, mechanisms and biotechnological applications. Heliyon. 2024;10(10). doi:10.1016/j.heliyon.2024.e31170
41. Abreu AP, Martins R, Nunes J. Emerging Applications of Chlorella sp. and Spirulina (Arthrospira) sp. Bioengineering. 2023;10(8):955. doi:10.3390/bioengineering10080955
42. Di Caprio F, Del Signore F, Capobianco L, Pagnanelli F, Altimari P. Feast–Famine in Cyclic Autotrophy/Heterotrophy Doubles Microalgal Productivity while Controlling Bacterial Contamination. ACS Sustain Chem Eng. 2025;13(39):16448-16458. doi:10.1021/acssuschemeng.5c05990
43. Youssef AM, Gomaa M, Mohamed AKSH, El-Shanawany ARA. Enhancement of biomass productivity and biochemical composition of alkaliphilic microalgae by mixotrophic cultivation using cheese whey for biofuel production. Environ Sci Pollut Res. 2024;31(30):42875-42888. doi:10.1007/s11356-024-33877-8
44. Castillo OS, Torres-Badajoz SG, Núñez-Colín CA, et al. Producción de biodiésel a partir de microalgas: avances y perspectivas biotecnológicas. Hidrobiológica. 2017;27(3):337-352.
45. Braun JCA, Balbinot L, Beuter MA, Rempel A, Colla LM. Mixotrophic cultivation of microalgae using agro-industrial waste: Tolerance level, scale up, perspectives and future use of biomass. Algal Res. 2024;80:103554. doi:10.1016/j.algal.2024.103554
46. Feng L, Guo W, Guo J, et al. FIB-SEM analysis on three-dimensional structures of growing organelles in wild Chlorella sp. pyrenoidosa cells. Protoplasma. 2023;260(3):885-897. doi:10.1007/s00709-022-01821-7
47. Chen H, Zheng Y, Zhan J, He C, Wang Q. Comparative metabolic profiling of the lipid-producing green microalga Chlorella sp. reveals that nitrogen and carbon metabolic pathways contribute to lipid metabolism. Biotechnol Biofuels. 2017;10(1):153. doi:10.1186/s13068-017-0839-4
Received: Marzo 10, 2026 / Accepted: Abril 21, 2026 / Published (Online First): Abril 22, 2026 / Issue Date: June 15, 2026 (Europe/Madrid)
Citation: Guevara Figueroa GE, Morales Avendaño ED, Rachid Romero Saker PJ, Vélez Espinoza JJ. Optimización del Crecimiento Mixotrófico de Chlorella sp. mediante la Valorización de Derivados Lácteos: Análisis Cinético, Bromatológico y de Costos. BioNatura Journal: Ibero-American Journal of Biotechnology and Life Sciences. 2026;3(2):6. https://doi.org/10.70099/BJ/2026.03.02.6
Correspondence should be addressed to: edmorales@espam.edu.ec
Peer Review Information: BioNatura Journal thanks the anonymous reviewers for their valuable contribution to the peer-review process. Regional peer-review coordination was conducted under the BioNatura Institutional Publishing Consortium (BIPC). Reviewer selection and assignment were supported via: https://www.reviewercredits.com/
Digital Preservation and Repository: This journal is managed through the Open Journal Systems (OJS) platform. To ensure long-term access, we use the PKP Preservation Network (PKP PN) to digitally preserve all published volumes in a decentralized, secure archive. Furthermore, our repository is integrated with LOCKSS and CLOCKSS, allowing international library networks to create permanent archives for long-term survival.
Citation: Guevara Figueroa GE, Morales Avendaño ED, Rachid Romero Saker PJ, Vélez Espinoza JJ. Optimización del Crecimiento Mixotrófico de Chlorella sp. mediante la Valorización de Derivados Lácteos: Análisis Cinético, Bromatológico y de Costos. BioNatura Journal: Ibero-American Journal of Biotechnology and Life Sciences. 2026;3(2):6. https://doi.org/10.70099/BJ/2026.03.02.6
Correspondence should be addressed to: edmorales@espam.edu.ec
Peer Review Information: BioNatura Journal thanks the anonymous reviewers for their valuable contribution to the peer-review process. Regional peer-review coordination was conducted under the BioNatura Institutional Publishing Consortium (BIPC). Reviewer selection and assignment were supported via: https://www.reviewercredits.com/
Digital Preservation and Repository: This journal is managed through the Open Journal Systems (OJS) platform. To ensure long-term access, we use the PKP Preservation Network (PKP PN) to digitally preserve all published volumes in a decentralized, secure archive. Furthermore, our repository is integrated with LOCKSS and CLOCKSS, allowing international library networks to create permanent archives for long-term survival.
Publisher Information: Published by Clinical Biotec S.L. (Madrid, Spain) as the publisher of record under the BioNatura Institutional Publishing Consortium (BIPC). Places of publication: Madrid (Spain); Tegucigalpa (Honduras); Panama City (Panama). Online ISSN: 3020-7886.